Перейти к:
Результаты остеосинтеза бедренной кости пластинами у пациентки с несовершенным остеогенезом
https://doi.org/10.14341/osteo13189
Аннотация
Несовершенный остеогенез — это редкое заболевание, характеризующееся хрупкостью костей, частыми переломами, костными деформациями, низкой минеральной плотностью кости. Относительный риск переломов костей у пациентов с несовершенным остеогенезом в 4–6 раз выше по сравнению с общей популяцией. У взрослых пациентов с несовершенным остеогенезом частота переломов диафиза бедренной кости примерно в 35 раз выше, чем в общей популяции. По современным литературным данным, предпочтительным методом остеосинтеза у таких пациентов является внутрикостный. Остеосинтез пластинами сопряжен с высокой частотой осложнений. Представлен случай лечения пациентки с несовершенным остеогенезом, которая с интервалом 2,5 года перенесла две операции остеосинтеза бедренной кости пластинами. Первая операция выполнялась по поводу перелома диафиза бедренной кости на высоте варусной деформации. Второй остеосинтез выполнялся по поводу периимплантного перелома проксимального отдела бедренной кости. Достигнута консолидация бедренной кости на обоих уровнях. Представленный случай демонстрирует, что накостный остеосинтез может быть эффективен при лечении переломов бедренной кости у пациентов с несовершенным остеогенезом с достижением консолидации при соблюдении описанных хирургических нюансов
Для цитирования:
Шевырев К.В., Шавырин Д.А., Мартыненко Д.В., Проскурина Е.В., Волошин В.П., Кондалева Р.В., Шахова М.А. Результаты остеосинтеза бедренной кости пластинами у пациентки с несовершенным остеогенезом. Остеопороз и остеопатии. 2025;28(1):38-47. https://doi.org/10.14341/osteo13189
For citation:
Shevyrev K.V., Shavyrin D.A., Martynenko D.V., Proskurina E.V., Voloshin V.P., Kondaleva R.V., Shakhova M.A. Results of plate osteosynthesis of the femur at the patient with osteogenesis imperfecta. Osteoporosis and Bone Diseases. 2025;28(1):38-47. (In Russ.) https://doi.org/10.14341/osteo13189
АКТУАЛЬНОСТЬ
Несовершенный остеогенез (незавершенный остеогенез, osteogenesis imperfecta, болезнь Лобштейна–Вролика, несовершенное костеобразование, болезнь «хрустального человека», далее — НО) — это редкое (орфанное) заболевание, характеризующееся хрупкостью костей, частыми переломами, костными деформациями, низкой минеральной плотностью кости, нарушением ее микроархитектоники и другими изменениями в органах, связанными с дефектом соединительной ткани. Этиология НО связана с наличием мутаций, приводящих к дисплазии соединительной ткани, что приводит к нарушению формирования костей, зубов, наличию изменений в различных органах и системах. В проведенных генетических исследованиях более чем в 90% случаев мутации обнаружены в генах коллагена COL1A1 и COL1A2 с аутосомно-доминантным типом наследования, в остальных 10% — мутации в генах белков, участвующих в биосинтезе и сборке молекулы коллагена, а также в генах шаперонов коллагена и гене остерикса, характеризующиеся аутосомно-рецессивным типом наследования. Кроме низкорослости и множественных переломов, у пациентов с НО могут отмечаться аномалии дентиногенеза, патология глаз, тугоухость, пороки сердечно-сосудистой и легочной систем и другие отклонения. Клинические проявления у членов семьи с аналогичными мутациями могут претерпевать значительную вариабельность.
Классификация НО с учетом гетерогенности клинических проявлений впервые была представлена в 1978 г. австралийским генетиком D. Sillence и описывала 4 варианта заболевания. С учетом развития генетической диагностики и обнаружения новых мутаций число типов НО увеличивается и в настоящее время насчитывает XVIII групп (по числу в соответствии с номерами генов, в которых выявлены мутации) [1]. Клиническая классификация Международной номенклатурной группы по изучению конституциональных нарушений скелета (INCDS) 2009 г. выделяет 5 основных групп. Классификация, предложенная Зариповой А.Р. и Хусаиновой Р.И. в 2020 г. и представленная в таблице 1, имеет соответствие клинической картины с результатами генетической диагностики, соответствует по основным разделам международной (INCDS) [2].
Таблица 1. Современная клиническая классификация несовершенного остеогенеза
|
Тип |
Название типа |
Ген |
Тип наследования (АД — аутосомно-доминантный; АР — аутосомно-рецессивный) |
|
I |
Недеформирующий тип с голубыми склерами |
COL1A1, COL1A2, SP7, BMP1, P3H1, PLS3 |
АД, X-сцепленный |
|
II |
Перинатально летальный, тяжелый |
COL1A1, COL1A2, CRTAP, P3H1, CREB3L1, PPIB, BMP1 |
АД, АР |
|
III |
Прогрессивно деформирующий, умеренно тяжелый |
COL1A1, COL1A2, BMP1, CRTAP, FKBP10, P3H1, PLOD2, PPIB, SERPINF1, SERPINH1, TMEM38B, WNT1, CREB3L1, FAM46A |
АД, АР |
|
IV |
Вариабельный НО с голубыми склерами, среднетяжелый |
COL1A1, COL1A2, WNT1, CRTAP, PPIB, SP7, PLS3, TMEM38B, FKBP10, SPARC |
AД, АР, X-сцепленный |
|
V |
Среднетяжелый НО с оссификацией межкостной мембраны предплечья |
IFITM5 |
AД |
Частота несовершенного остеогенеза в разных странах при рождении колеблется, в среднем составляет 6–7 случаев на 100 тысяч новорожденных, в Российской Федерации, по данным Федерального регистра 2015 г., в среднем по стране 1–1,5 на 100 тысяч новорожденных [3].
Высокая частота переломов при НО была признана с момента первого медицинского описания этого заболевания в 1690 г., но эпидемиология переломов на протяжении жизни была описана недавно [4]. Популяционное исследование в Дании показало, что люди с диагнозом НО имеют в восемь раз более высокую частоту переломов (все участки скелета вместе взятые), чем общая популяция [5]. Относительный риск переломов при НО по сравнению с общей популяцией значительно варьировался с возрастом (в 11 раз выше у людей с НО моложе 20 лет, в 6 раз — от 20 до 54 лет и в 4 раза у людей в возрасте 55 лет и старше). Как и в общей популяции, у женщин с НО наблюдалась более высокая частота переломов во время менопаузы, чем у женщин в пременопаузе.
У взрослых с НО частота переломов диафиза бедренной кости примерно в 35 раз выше, чем в общей популяции [6].
Хирургическое лечение переломов у пациентов с НО является сложной задачей и сопряжено с низкой минеральной плотностью костной ткани, уже существующими деформациями скелета, изменениями костей и мягких тканей после уже перенесенных операций [7].
Современные литературные источники в большинстве случаев посвящены хирургическому лечению переломов и деформаций костей у детей с НО. Они не рекомендуют накостный остеосинтез из-за высокого числа неудовлетворительных результатов лечения и осложнений. Немногочисленные статьи, посвященные хирургическому лечению переломов и коррекции деформаций у взрослых пациентов с несовершенным остеогенезом, также не рекомендуют применять накостные фиксаторы [8][9][10]. И лишь единичные работы сообщают об эффективности пластин при правильном учете возможных рисков периимплантных переломов [8].
В центре орфанных заболеваний ГБУЗ МО МОНИКИ им. М.Ф. Владимирского (далее — МОНИКИ) наблюдаются 58 пациентов (в том числе 15 детей) с диагнозом: «Несовершенный остеогенез» (код МКБ-10 Q78.0). В наблюдаемой группе — 30 пациентов мужского пола и 28 — женского, имеется 7 семей, в которых 2 и более пациентов с НО. Пациенты наблюдаются эндокринологом и травматологом-ортопедом, получают терапию препаратами группы бисфосфонатов, остеогенон, витамин Д и др. Проводится оценка степени минерализации скелета денситометрическим методом 1 раз в 1–2 года для коррекции проводимой терапии. При необходимости хирургической коррекции пациенты госпитализируются в отделение травматологии и ортопедии МОНИКИ.
ОПИСАНИЕ СЛУЧАЯ
22.01.2019 г. в отделение травматологии и ортопедии МОНИКИ госпитализирована пациентка Р. 32 лет с жалобами на боли в правом бедре, вынужденное положение правой нижней конечности и невозможность опоры на правую ногу.
Анамнез травмы: 01.01.2019 г. упала с высоты собственного роста, почувствовала резкую боль в правом бедре, обнаружила деформацию правого бедра. Бригадой скорой медицинской помощи доставлена в стационар по месту жительства. Во время рентгенологического исследования диагностирован периимплантный подвертельный перелом правой бедренной кости со смещением отломков. Наложено скелетное вытяжение, обследована, переведена для оперативного лечения в отделение травматологии и ортопедии МОНИКИ.
Анамнез жизни, основного заболевания и его осложнений: пациентка с младенчества страдает остеопорозом тяжелого течения, осложненным множественными патологическими переломами на фоне несовершенного остеогенеза и синдромом Элерса-Данлоса. Родилась от 1 беременности, при рождении: хроническая гипоксия, врожденная гидроцефалия, внутриутробный перелом левого бедра, левосторонняя косолапость. До 1 года жизни с отставанием физического и моторного развития, имели место гипохромная анемия I ст., нарушение костеобразования. Диагноз несовершенного остеогенеза установлен в 2-летнем возрасте.
С 16-летнего возраста (2003 г.) наблюдается в медико-генетическом центре МОНИКИ по поводу несовершенного остеогенеза 1 типа с аутосомно-доминантным типом наследования и синдрома Элерса-Данлоса. Несовершенный остеогенез диагностирован у матери пациентки. Имеет дочь 2013 г.р., которая также страдает несовершенным остеогенезом, перенесла несколько переломов и наблюдается в медико-генетическом центре МОНИКИ.
Генетическая диагностика пациентке не проводилась в связи с высокой стоимостью и невключением данного вида диагностики в программу госгарантий. Дочери пациентки при обследовании в федеральном центре было проведено молекулярно-генетическое исследование клинического экзома и выявлен нуклеотидный вариант с.3505G>А (chr17:50187041С>Т; NM_000088.4; rs67815019) в гетерозиготном состоянии в экзоне 47 гена COL1A1 (OMIM 120150), валидированный методом секвенирования по Сэнгеру, приводящий к аминокислотному варианту р. G1169S, не описанный в контрольной выборке gnomAD v4.1.0. Нуклеотидный вариант описан в международной базе HGMD professional [ CM070694] у пациентов с несовершенным остеогенезом, тип І, тип II, тип III. В соответствии с российским Руководством по интерпретации данных последовательности ДНК человека, выявленный нуклеотидный вариант следует расценивать как патогенный. Согласно базе данных ОМІМ, мутации в гене COL1A1 описаны у пациентов с несовершенным остеогенезом, тип І (ОММ 166200), тип ІI (ОМІМ 166210), тип III (ОМІМ 259420), тип IV (OMIM 166220), болезнью Каффи (ОМІМ 114000) и синдромом Элерса-Данлоса, тип артрохалазия (ОМІМ 130060), наследуемыми по аутосомно-доминантному типу. Таким образом, имеется генетическое подтверждение наличия мутации, вызываемой клинические признаки несовершенного остеогенеза у дочери пациентки. Данный результат генетического исследования с высокой вероятностью можно расценивать как идентичный у рассматриваемой пациентки (матери обследованной девочки).
При осмотре пациентки обнаруживаются макроцефалия, голубые склеры, нарушение дентиногенеза, множественные деформации костей нижних конечностей, сколиоз, плоскостопие, гипермобильность суставов, снижение слуха. В настоящее время во взрослом состоянии пациентка имеет рост 130 см, вес 70 кг.
В общей сложности пациентка перенесла 6 переломов: первый — внутриутробный перелом левого бедра, второй в возрасте 10 лет — перелом правого бедра, в 12 лет получила третий перелом — левого бедра (лечение оперативное — резекция ложного сустава левого бедра с коррекцией деформации и остеосинтезом), металлофиксаторы удалены. Четвертый перелом получила в возрасте 24 лет — перелом большеберцовой кости слева, лечилась консервативно. В 29 лет (02.05.2016 г.) получила пятый по счету перелом — закрытый поперечный перелом средней трети диафиза правой бедренной кости, по поводу которого 02.06.2016 г. выполнен компрессионный остеосинтез пластиной с блокированием (рис. 1–2).
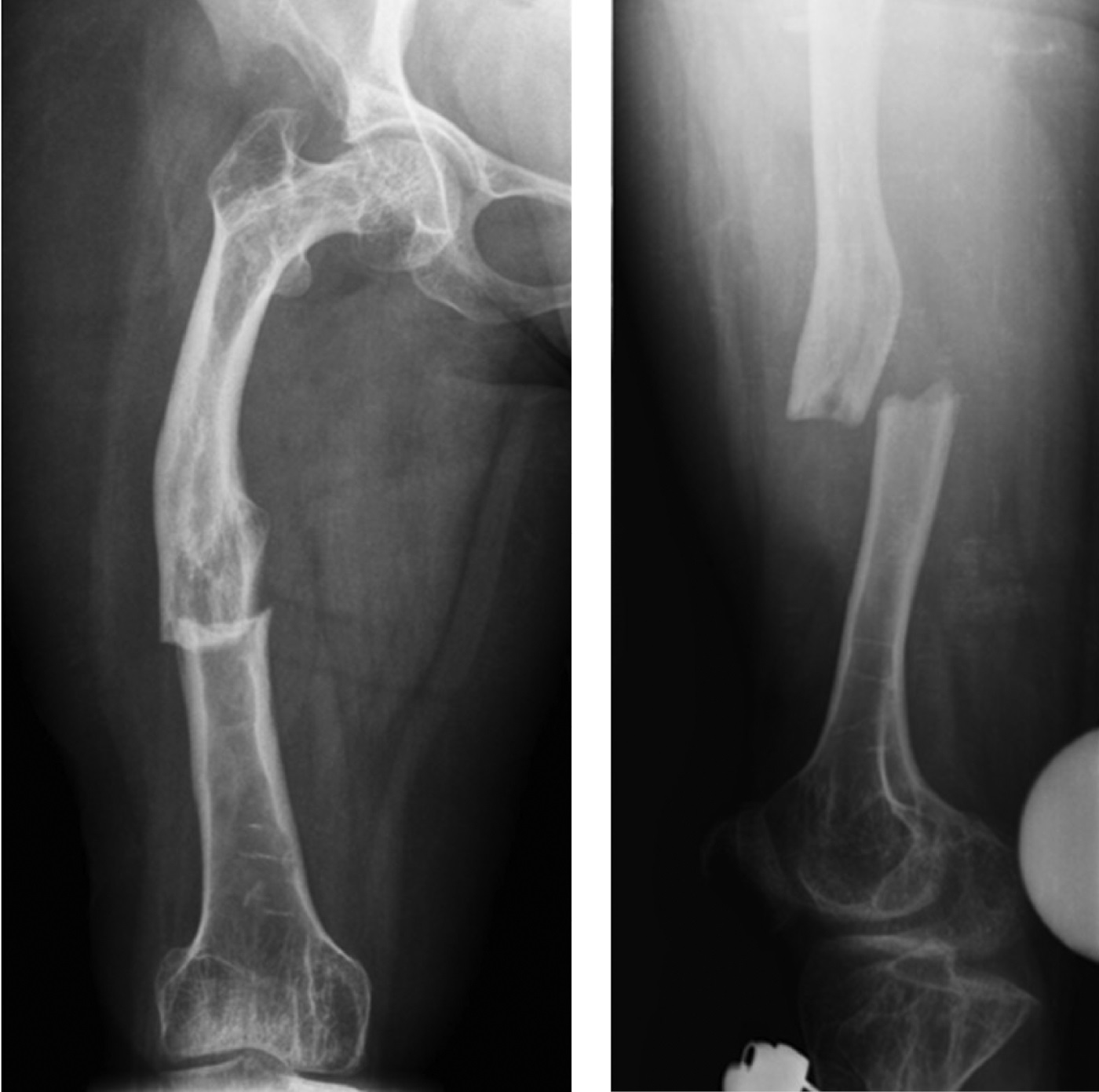
Рисунок 1. Рентгенограммы пациентки с переломом правой бедренной кости.

Рисунок 2. Рентгенограммы пациентки после остеосинтеза бедренной кости, блокируемой пластиной.
Во время этого вмешательства были выполнены открытая репозиция отломков с сохранением предсуществующей формы правой бедренной кости и компрессионный остеосинтез пластиной с блокированием. Для деконцентрации напряжения по краям фиксатора в надмыщелковой зоне бедренной кости использован неблокируемый бикортикальный винт 4,5 мм, а в проксимальном отделе блокируемый винт был введен по касательной, кпереди от дуги Адамса. Удаление имплантатов не планировалось. После консолидации кости на этом уровне в сроки 10 месяцев у пациентки восстановилась опороспособность конечности. Однако произошел периимплантный низкоэнергетический подвертельный перелом бедренной кости при падении на правый бок 01.01.2019 г.
При госпитализации пациентки в отделение травматологи ортопедии МОНИКИ установлено, что линия перелома проходила косо-поперечно через канал второго винта (рис. 3), на котором концентрировались изгибающие нагрузки из-за сохраняющейся варусной деформации проксимального отдела бедренной кости. К сожалению, проксимальный винт не обеспечил деконцентрацию нагрузки, что привело к усталостным изменениям кости и последующему перелому.

Рисунок 3. Рентгенограммы пациентки с периимплантным переломом бедренной кости.
В связи с этим после стационарного обследования 29 января 2019 г. была выполнена операция — удаление винтов и пластины из правого бедра, экономная адаптирующая резекция на уровне периимплантного перелома, корригирующая деваризация и компрессионный остеосинтез блокируемой пластиной. Для остеосинтеза использовалась «перевернутая» контрлатеральная дистальная бедренная пластина в режиме динамической компрессии двумя кортикальными винтами. Для деконцентрации напряжения был использован монокортикальный дистальный винт. С учетом сниженной минеральной плотности кости количество винтов, введенных в каждый отломок, было больше, чем при остеосинтезе бедренной кости без остеопороза (рис. 4).
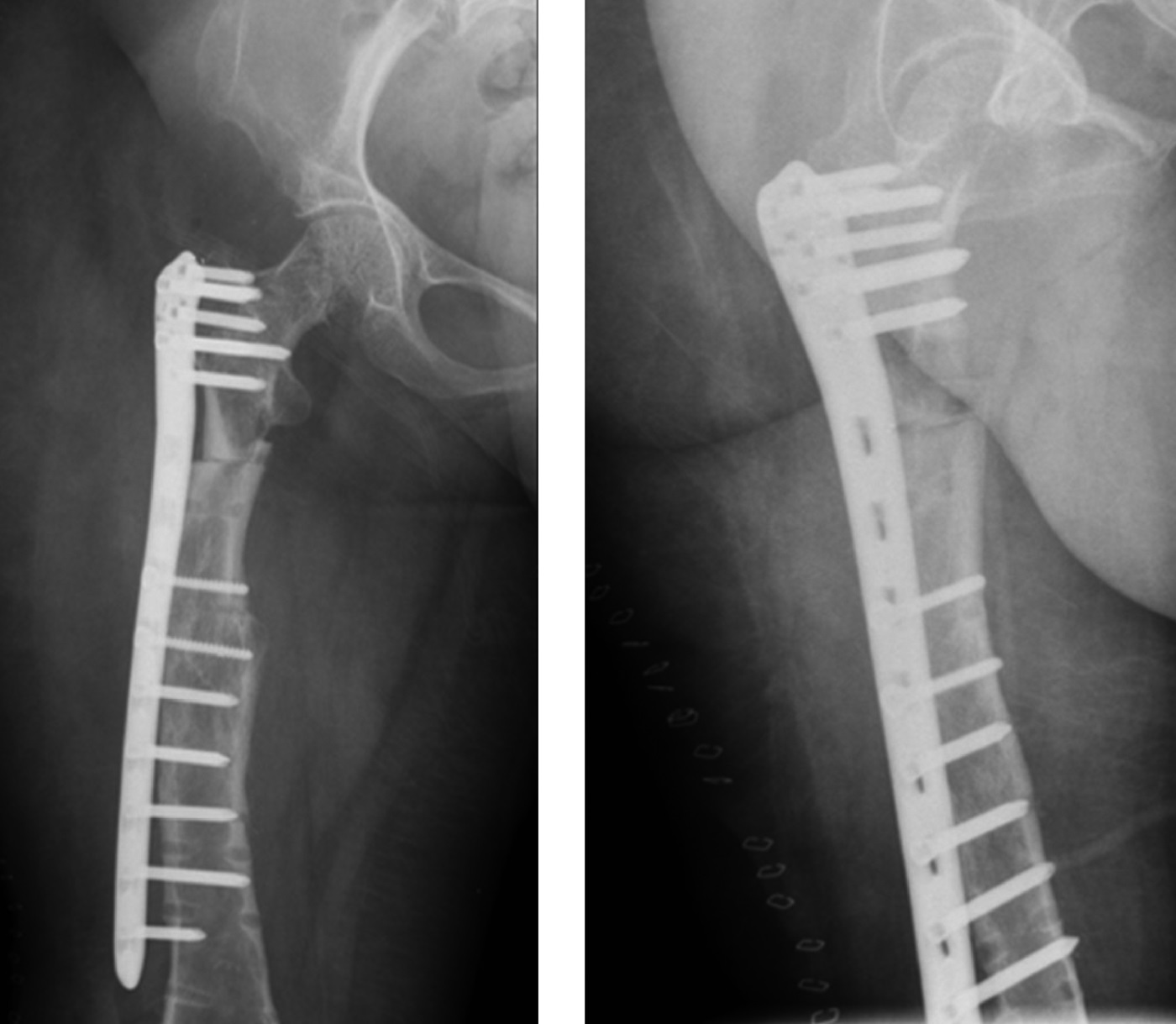
Рисунок 4. Рентгенограммы пациентки после операции удаления имплантатов, корригирующей остеотомии проксимального отдела правой бедренной кости и остеосинтеза блокируемой пластиной.
В послеоперационном периоде пациентка наблюдалась амбулаторно у генетика, эндокринолога и травматолога-ортопеда МОНИКИ. В процессе наблюдения отмечена положительная рентгенологическая динамика сращения (рис. 5).
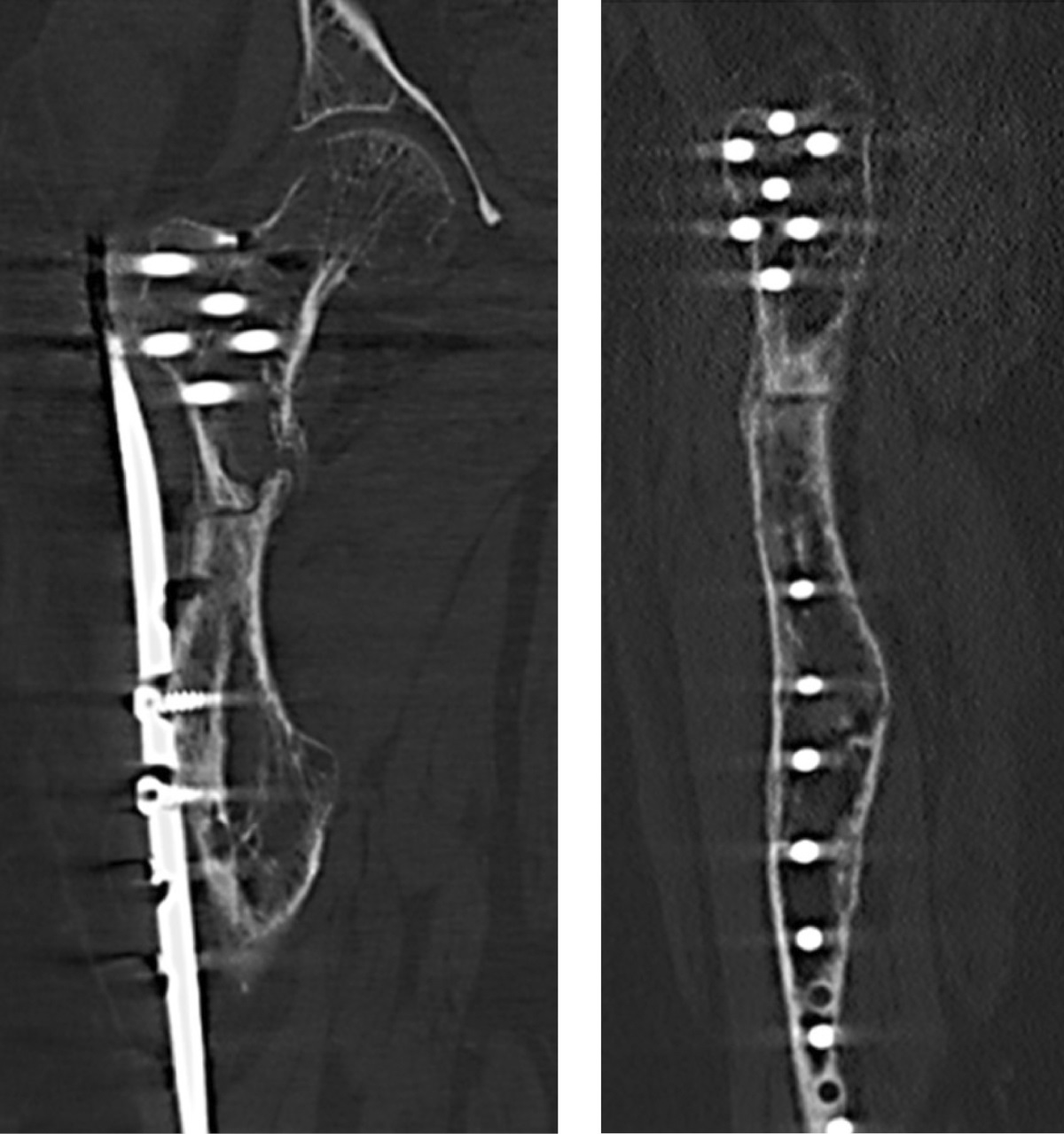
Рисунок 5. МСКТ-срезы правой бедренной кости пациентки через полгода после операции с признаками периостального мозолеобразования.
РЕЗУЛЬТАТЫ ФИЗИКАЛЬНОГО, ЛАБОРАТОРНОГО И ИНСТРУМЕНТАЛЬНОГО ИССЛЕДОВАНИЙ
Динамика лабораторных показателей:
- биохимический анализ крови (январь 2019 г.): холестерин — 3,0 ммоль/л, альбумин — 30 г/л, мочевина — 7 ммоль/л, креатинин — 43 мкмоль/л, глюкоза — 4,7 ммоль/л, кальций — 2,2 мкмоль/сут (норма 2,15–2,79 мкмоль/сут);
- биохимический анализ крови (январь 2022 г.): глюкоза — 4,6 ммоль/л, креатинин — 60 мкмоль/л, мочевина — 2,2 ммоль/л, кальций — 2,19 мкмоль/сут (норма 2,15–2,79 мкмоль/сут.);
- биохимический анализ крови (январь 2023 г.): креатинин — 57,74 мкмоль/л, мочевина — 2,99 ммоль/л, глюкоза — 3.52 ммоль/л, кальций — 2,5 мкмоль/сут (норма 2,15–2,79 мкмоль/сут);
- денситометрия (сентябрь 2022 г.): в шейке левой бедренной кости минеральная плотность кости составляет 88% от возрастной нормы (Z-критерий -0,9 SD).
В бедре Z-критерий -2,3 SD. В дистальном отделе костей предплечья минеральная плотность кости справа составляет 107% от возрастной нормы (Z-критерий +0,8 SD).
Назначаемую эндокринологом с 2016 г. остеотропную терапию (постоянный прием комбинированных препаратов кальция и витамин D3, золендроновую кислоту 5 мг внутривенно капельно на физиологическом растворе 1 раз в год) получала нерегулярно. Так, пациентка впервые и единственный раз получила золендроновую кислоту в 2022 г.
ИСХОД И РЕЗУЛЬТАТЫ НАБЛЮДЕНИЯ
Последнее обращение к травматологу-ортопеду в ноябре 2023 г. было связано с тотальной нестабильностью левого коленного сустава смешанного генеза (гипермобильность и травма) на фоне гонартроза. Из-за нестабильности левого коленного сустава пациентка передвигается при помощи костылей, ограничивая нагрузку преимущественно на левую нижнюю конечность, и использует полужесткий ортез для коленного сустава. Подвижность в правых коленном и тазобедренном суставах ограничена углом 90 градусов (рис. 6).
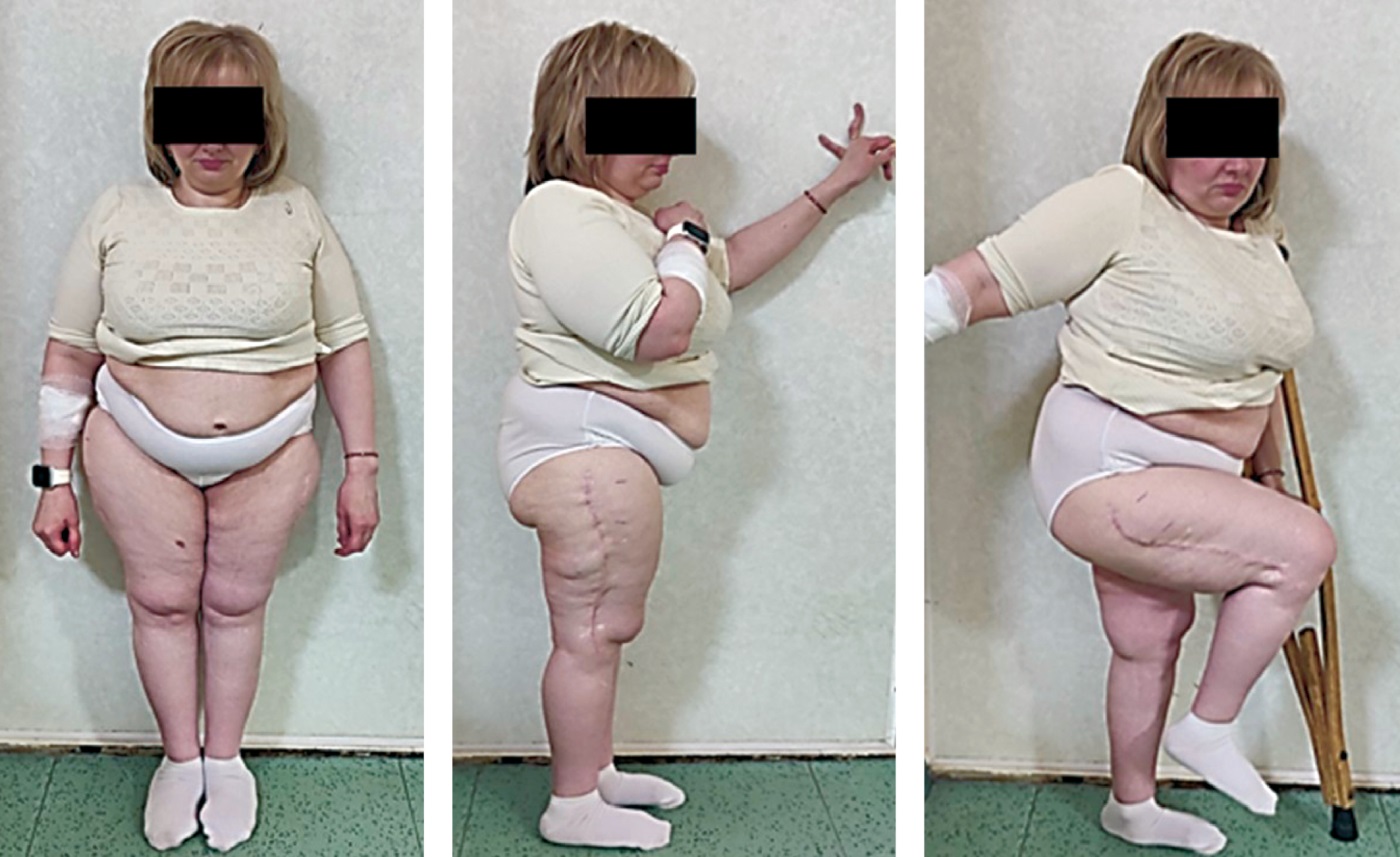
Рисунок 6. Внешний вид пациентки через 5 лет и 4 месяца после оперативного вмешательства на правом бедре.
Несмотря на достигнутую консолидацию перелома проксимального отдела правой бедренной кости, рентгенологически прослеживается его зона, что характерно для НО (рис. 7). Ось оперированной бедренной кости близка к оси здоровой кости (рис. 8).
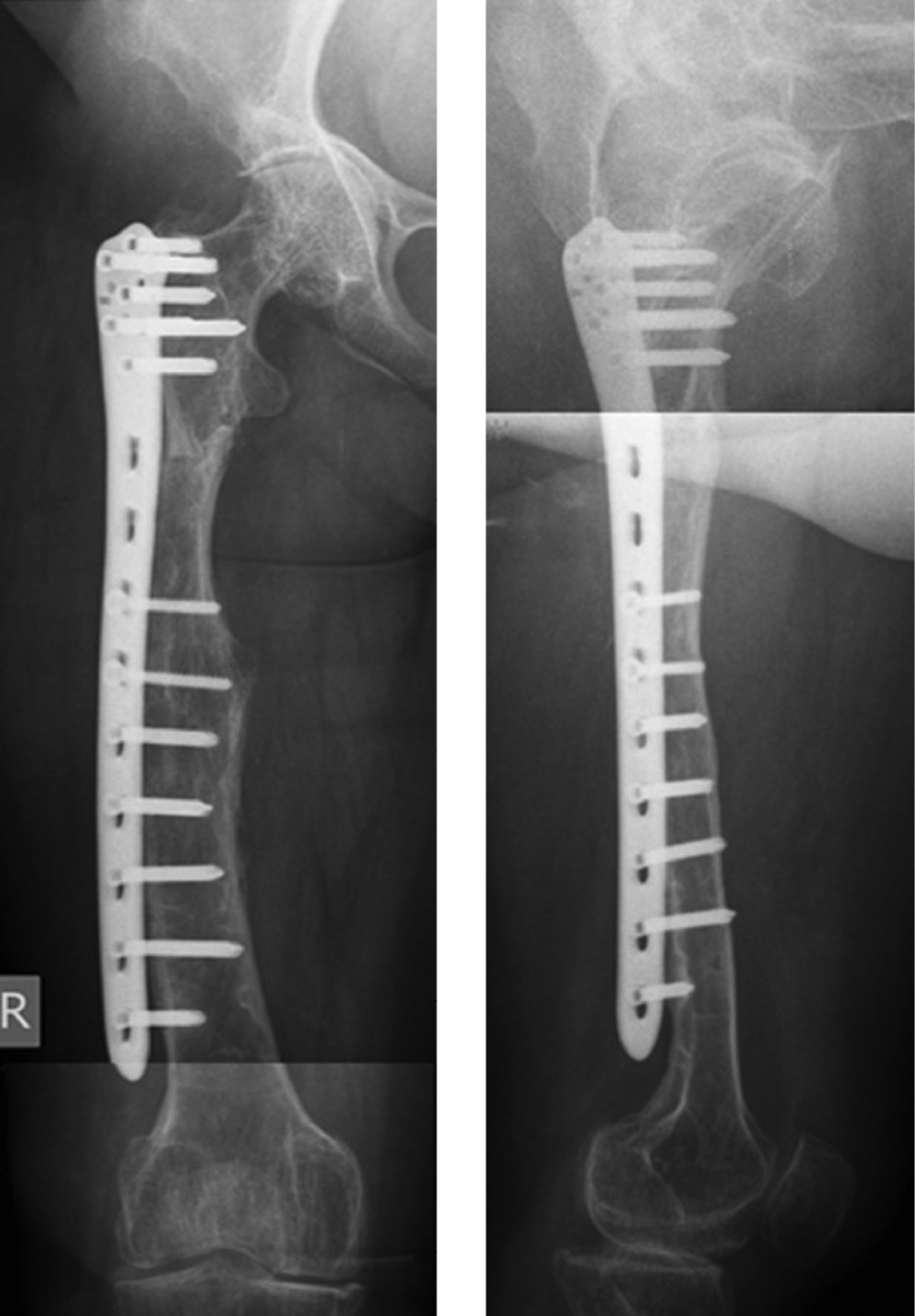
Рисунок 7. Рентгенограммы правой бедренной кости пациентки 5 лет и 4 месяца после оперативного вмешательства.

Рисунок 8. Осевые рентгенограммы нижних конечностей через 5 лет и 4 месяца после оперативного вмешательства на правом бедре.
ОБСУЖДЕНИЕ
Низкая механическая прочность кости на фоне остеопении, повышенная чувствительность кости к знакопеременным нагрузкам, пластическая или посттравматическая деформация сегмента отягощают прогноз и требуют специальных подходов к лечению переломов у пациентов с НО. Нередко у таких пациентов взрослого возраста отмечается неполное сращение перелома либо формирование однокортикальной щели [8]. Нарушение процессов физиологического и репаративного остеогенеза на генетическом уровне не может быть преодолено при современном состоянии медицины. Поэтому выбор имплантатов для остеосинтеза у пациентов с НО, получивших перелом бедренной кости, а также при операции корригирующей остеотомии представляет известную сложность. Тем более, что сохраняющаяся у пациентов неполноценность кости ставит под сомнение целесообразность их последующего удаления.
Большинство авторов, демонстрирующие как свой опыт, так и ссылающиеся на опыт и рекомендации коллег, не рекомендуют применение пластин [8]. Так, Мингазов Э.Р. с соавт. сообщают, что применение накостных пластин, винтов при тяжелых формах несовершенного остеогенеза в настоящее время неактуально [9]. Enright с соавт. сообщают о полученных 69,2% осложнений при использовании накостных имплантатов у пациентов с НО и рекомендуют отказаться от них в пользу внутрикостной фиксации [10]. В мае 2016 г. группой американских авторов опубликована обзорная статья с рекомендациями по ортопедическому лечению взрослых пациентов с несовершенным остеогенезом. Авторы рекомендуют избегать использования блокируемых пластин и чрезмерно жесткой фиксации костей у этих пациентов [11].
Лишь в единичных публикациях сообщается о возможности эффективного применения накостных пластин при фиксации перелома или корригирующей остеотомии у взрослых пациентов с НО и даются рекомендации по их безопасному применению [7].
В литературе нам встретились случаи фиксации переломов бедренной кости у взрослых пациентов с НО интрамедуллярным эластичным стержнем [12] и фотодинамическим интрамедуллярным гвоздем [13]. К сожалению, в обоих случаях развились периимплантные переломы. Лечение периимплантного перелома у пациента с эластичным стержнем проводилось консервативно. Пациенту с фотодинамическим штифтом выполнен накостный остеосинтез. В обоих случаях получен положительный результат лечения.
Небольшое количество взрослых пациентов с переломами при НО не позволяет исследователям набрать достаточные статистические группы, чтобы подтвердить преимущества интрамедуллярного и возможности накостного остеосинтеза в зависимости от уровня перелома и сопутствующей деформации бедренной кости при НО.
Представленный клинический случай еще раз заставляет задуматься хирургов-ортопедов над выбором имплантата для остеосинтеза бедренной кости у взрослых пациентов с НО. Оптимальный металлофиксатор для остеосинтеза бедренной кости у пациентов с НО не должен создавать зоны локальной перегрузки и ремоделирования костной ткани по концам фиксатора. Поэтому в нашем случае при первичном остеосинтезе накостной пластиной предпринята попытка деконцентрировать напряжение за счет проведения проксимального блокируемого винта по касательной к поперечнику кости. При этом не учтено, что упругие деформации из-за варусной формы проксимального отдела бедренной кости, оставленной при первичном остеосинтезе, могут способствовать быстрой дестабилизации кортикального винта, а следовательно — концентрации напряжений в непосредственной близости от жестко блокированного бикортикального винта и последующему усталостному перелому.
Наиболее равномерно нагрузки на бедренную кость распределяются при остеосинтезе интрамедуллярными металлофиксаторами, поэтому большинство авторов, как указано выше, считает их применение оптимальным в условиях НО [8][9][10].
Однако при НО характерным является выраженная дугообразная деформация бедренного канала на всем протяжении, нередко сопровождающимся угловыми деформациями в другой плоскости из-за предшествующих переломов. В зависимости от степени и протяженности деформации введение интрамедуллярного штифта в некоторых ситуациях оказывается невозможным без проведения дополнительной (одной или нескольких) остеотомии. Так, при переломе в подвертельной области протяженное искривление бедренного канала затрудняет применение интрамедуллярного металллофиксатора без остеотомии бедренной кости на высоте ее деформации. Если существует возможность исправить механическую ось сегмента за счет коррекции (гиперкоррекции) по линии перелома, оправдано применение премоделированных накостных пластин, которые не требуют проведения дополнительных остеотомий кости вне перелома. Риски формирования «концевой» локальной перегрузки и ремоделирования костной ткани в таком случае представляются сопоставимыми с таковыми от блокирующих элементов интрамедуллярного фиксатора.
ЗАКЛЮЧЕНИЕ
Представленный нами случай демонстрирует, что накостный остеосинтез может быть эффективен при лечении переломов бедренной кости у пациентов с НО с достижением консолидации. Продемонстрированный случай подтверждает литературные данные о вероятности развития после остеосинтеза пластинами периимплантных переломов, что обусловлено созданием концентраторов напряжения (винты, край пластины), сниженной костной массой, предсуществующей деформацией. При возможности во время операции остеосинтеза нужно стараться максимально устранить деформацию бедренной кости (чаще варусно-флексионную). Длина накостного имплантата должна достигать метафизарных зон проксимально и дистально, насколько это позволяет деформация. Крайние винты в пластине не должны служить концентраторами напряжения из-за опасности периимплантного перелома. Они должны быть монокортикальными блокируемого или кортикального типа. Возможен вариант введения бикортикального винта, но кортикального типа. Показания к удалению пластины после консолидации бедренной кости у пациентов с несовершенным остеогенезом, особенно при сохраняющейся деформации, лучше ограничить периимплантной инфекцией.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источники финансирования. Работа выполнена по инициативе авторов без привлечения финансирования.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Согласие пациента. Пациент добровольно подписал информированное согласие на публикацию персональной медицинской информации в обезличенной форме.
Список литературы
1. Marini JC, Forlino A, Cabral WA, Barnes AM, San Antonio JD, et al. Consortium for osteogenesis imperfecta mutations in the helical domain of type I collagen: regions rich in lethal mutations align with collagen binding sites for integrins and proteoglycans. Hum Mutat. 2007;28(3):209-21. doi: https://doi.org/10.1002/humu.20429
2. Зарипова А.Р., Хусаинова Р.И. Современная классификация и молекулярно-генетические аспекты незавершенного остеогенеза. // Вавиловский журнал генетики и селекции. — 2020. — Т.24. — №2. — С.219-227.
3. Яхяева Г.Т., Намазова-Баранова Л.С., Маргиева Т.В. Новые аспекты генетической основы, классификации и лечения несовершенного остеогенеза: литературный обзор. // Педиатрическая фармакология. — 2015. — Т. 12. — №5. — С.579-588.
4. Charlier P, Perciaccante A, Bianucci R. Oldest medical description of osteogenesis imperfecta (17th Century, France). Clin Anat. 2017;30:128–9. doi: https://doi.org/10.1002/ca.22806
5. Folkestad L, Hald JD, Ersboll AK, et al. Fracture rates and fracture sites in patients with osteogenesis imperfecta: a nationwide register-based cohort study. J Bone Miner Res. 2017;32:125–34. doi: https://doi.org/10.1002/jbmr.2920
6. Goudriaan WA, Harsevoort GJ, van Leeuwen M, Franken AA, Janus GJM. Incidence and treatment of femur fractures in adults with osteogenesis imperfecta: an analysis of an expert clinic of 216 patients. Eur J Trauma Emerg Surg. 2018. doi: https://doi.org/10.1007/s00068-018-1005-9
7. Gil JA, DeFroda SF, Sindhu K, Cruz AI Jr, Daniels AH. Challenges of Fracture Management for Adults With Osteogenesis Imperfecta. Orthopedics. 2017;40(1):e17-e22. doi: https://doi.org/10.3928/01477447-20161006-04
8. Cho TJ, Ko JM, Kim H, Shin HI, Yoo WJ, Shin CH. Management of Osteogenesis Imperfecta: A Multidisciplinary Comprehensive Approach. Clin Orthop Surg. 2020;12(4):417-429. doi: https://doi.org/10.4055/cios20060
9. Мингазов Э.Р., Чибиров Г.М., Попков Д.А. Ортопедические осложнения и ятрогении при коррекции деформаций нижних конечностей у пациентов, страдающих тяжелыми формами несовершенного остеогенеза // Гений ортопедии. — 2018. — Т. 24. — № 2. — С. 168-176. doi: https://doi.org/10.18019/1028-4427-2018-24-2-168-176
10. Enright WJ, Noonan KJ. Bone plating in patients with type III osteogenesis imperfecta: results and complications. Iowa Orthop J. 2006;26:37-40
11. Roberts TT, Cepela DJ, Uhl RL, Lozman J. Orthopaedic Considerations for the Adult With Osteogenesis Imperfecta. J Am Acad Orthop Surg. 2016;24(5):298-308. doi: https://doi.org/10.5435/JAAOS-D-15-00275
12. Ballhause TM, Gessler R, Priemel MH, Frosch KH, Schlickewei CW. Osteosynthesis of a Multifragment Femoral Shaft Fracture and Peri-Implant Refracture in an 83-Year-Old Patient with Osteogenesis Imperfecta. Case Rep Orthop. 2020;2020:8887644. doi: https://doi.org/10.1155/2020/8887644
13. Fourman MS, Rothenberg AC, McGough RL, Weiss KR, Goodman MA. Standalone Photodynamic Intramedullary Implants in the Treatment of Bilateral Refractory Femoral Nonunions in a Patient with Osteogenesis Imperfecta: Significant Utility in Load-Bearing Bones, But Not a Replacement for Biomechanical Optimization. Oper Tech Orthop. 2020. doi: https://doi.org/10.1016/j.oto.2020.100805
Об авторах
К. В. ШевыревРоссия
Шевырев Константин Васильевич, к.м.н., ведущий научный сотрудник отделения травматологии и ортопедии и доцент кафедры травматологии и ортопедии
129110, г. Москва, ул. Щепкина 61/2
AuthorID: 479881
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Д. А. Шавырин
Россия
Шавырин Дмитрий Александрович, д.м.н.
129110, г. Москва, ул. Щепкина 61/2
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Д. В. Мартыненко
Россия
Мартыненко Дмитрий Владимирович, к.м.н., доцент
129110, г. Москва, ул. Щепкина 61/2
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Е. В. Проскурина
Россия
Проскурина Елена Валерьевна
129110, г. Москва, ул. Щепкина 61/2
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
В. П. Волошин
Россия
Волошин Виктор Парфентьевич, д.м.н., профессор
129110, г. Москва, ул. Щепкина 61/2
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Р. В. Кондалева
Россия
Кондалева Регина Владимировна
129110, г. Москва, ул. Щепкина 61/2
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
М. А. Шахова
Россия
Шахова Маргарита Алексеевна
129110, г. Москва, ул. Щепкина 61/2
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Дополнительные файлы
|
|
1. Рисунок 1. Рентгенограммы пациентки с переломом правой бедренной кости. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(705KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 2. Рентгенограммы пациентки после остеосинтеза бедренной кости, блокируемой пластиной. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(480KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 3. Рентгенограммы пациентки с периимплантным переломом бедренной кости. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(517KB)
|
Метаданные ▾ | |
|
|
4. Рисунок 4. Рентгенограммы пациентки после операции удаления имплантатов, корригирующей остеотомии проксимального отдела правой бедренной кости и остеосинтеза блокируемой пластиной. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(454KB)
|
Метаданные ▾ | |
|
|
5. Рисунок 5. МСКТ-срезы правой бедренной кости пациентки через полгода после операции с признаками периостального мозолеобразования. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(630KB)
|
Метаданные ▾ | |
|
|
6. Рисунок 6. Внешний вид пациентки через 5 лет и 4 месяца после оперативного вмешательства на правом бедре. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(1009KB)
|
Метаданные ▾ | |
|
|
7. Рисунок 7. Рентгенограммы правой бедренной кости пациентки 5 лет и 4 месяца после оперативного вмешательства. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(457KB)
|
Метаданные ▾ | |
|
|
8. Рисунок 8. Осевые рентгенограммы нижних конечностей через 5 лет и 4 месяца после оперативного вмешательства на правом бедре. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(618KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Шевырев К.В., Шавырин Д.А., Мартыненко Д.В., Проскурина Е.В., Волошин В.П., Кондалева Р.В., Шахова М.А. Результаты остеосинтеза бедренной кости пластинами у пациентки с несовершенным остеогенезом. Остеопороз и остеопатии. 2025;28(1):38-47. https://doi.org/10.14341/osteo13189
For citation:
Shevyrev K.V., Shavyrin D.A., Martynenko D.V., Proskurina E.V., Voloshin V.P., Kondaleva R.V., Shakhova M.A. Results of plate osteosynthesis of the femur at the patient with osteogenesis imperfecta. Osteoporosis and Bone Diseases. 2025;28(1):38-47. (In Russ.) https://doi.org/10.14341/osteo13189

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).






































