Перейти к:
Оценка эффективности терапии бисфосфонатами взрослых пациентов с несовершенным остеогенезом
https://doi.org/10.14341/osteo13210
Аннотация
Обоснование: Несовершенный остеогенез (НО) — это редкое наследственное заболевание соединительной ткани, характеризующееся снижением плотности костной ткани и рецидивирующими низкотравматическими переломами. На сегодняшний день бисфосфонаты (БФ) при НО используются с целью увеличения плотности кости и снижения количества новых переломов, однако имеющиеся данные касаются преимущественно использования БФ у детей. При этом, благодаря раннему началу антирезорбтивной терапии, все большее количество пациентов с НО достигают совершеннолетия, что требует определения показаний и оценки эффективности терапии БФ у взрослых пациентов с НО.
Цель исследования: Оценка эффективности терапии бисфосфонатами у взрослых пациентов с несовершенным остеогенезом.
Материалы и методы: Проведено продольное сравнительное исследование 45 пациентов с НО на базе клиники Башкирского государственного медицинского университета. 24 пациента однократно получили золедроновую кислоту 5мг/100 мл внутривенно капельно. Минеральная плотность костной ткани (МПК) определялась при помощи рентгеновской денситометрии. Уровень болевого синдрома оценивался при помощи визуально-аналоговой шкалы. Оценка дисплазии соединительной ткани (ДСТ) проводилась по модифицированной таблице Т.И. Кадуриной.
Результаты: Статистически значимые различия наблюдались при сравнении ИМТ у пациентов с I и III (23,6±4,6; 28,5±5,9; p=0,0183), I и V (23,6±4,6; 30,8±8,2; p=0,014) типами НО. Статистически значимых различий уровней балльно-количественной оценки ДСТ, болевого синдрома по ВАШ и z-критерия между разными типами заболевания не наблюдалось. У пациентов, получивших БФ в КБГМУ наблюдалось статистически значимое уменьшение болевого синдрома (p<0,0001) и увеличение уровня z-критерия (p=0,045) через год после введения препарата, независимо от наличия лечения бисфосфонатами ранее. При проведении корреляционного анализа у пациентов с НО обнаружена умеренная обратная связь между МПК и количеством переломов (r=-0,488, p=0,001), умеренная прямая связь между степенью выраженности ДСТ и уровнем болевого синдрома (r=0,408, p=0,005). Количество переломов также коррелировало с ИМТ (r=0,337, p=0,024).
Заключение: У взрослых пациентов с НО сохраняются низкие уровни показателей МПК и z-критерия, и присутствует умеренный постоянный болевой синдром в костях, не связанный с переломами. Интенсивность данных показателей не зависит от наличия предыдущей терапии бисфосфонатами. Лечение БФ является эффективным, так как наблюдалось статистически значимое увеличение МПК и z-критерия по результатам денситометрии, и статистически значимое уменьшение уровня болевого синдрома в костях. Основными показаниями для введения БФ являются: наличие переломов в течение года, низкие показатели денситометрии (z-критерий<-2,0), наличие умеренного постоянного болевого синдрома в костях (ВАШ>5 баллов).
Ключевые слова
Для цитирования:
Валеева Д.И., Хусаинова Р.И., Тюрин A.B. Оценка эффективности терапии бисфосфонатами взрослых пациентов с несовершенным остеогенезом. Остеопороз и остеопатии. 2025;28(3):4-11. https://doi.org/10.14341/osteo13210
For citation:
Valeeva D.I., Khusainova R.I., Tiurin A.V. Evaluation of the efficacy of bisphosphonate therapy in adult patients with osteogenesis imperfecta. Osteoporosis and Bone Diseases. 2025;28(3):4-11. (In Russ.) https://doi.org/10.14341/osteo13210
ОБОСНОВАНИЕ
Несовершенный остеогенез (незавершенный остеогенез, НО, МКБ-10: Q78.0) — это наследственное заболевание, характеризующееся хрупкостью костей и повышенным риском переломов [1]. Среди других орфанных скелетных патологий данное заболевание является наиболее распространенным и встречается с частотой 1:15–20 000 новорожденных [2]. Около 90% случаев НО вызваны мутациями в генах, кодирующих коллаген I типа (COL1A1 или COL1A2), являющийся основным компонентом внеклеточного матрикса кости. Мутации в генах, связанных с модификацией коллагена (CRTAP, LEPRE1 и PPIB), сборкой и везикулярным транспортом коллагена (SERPINH1 и FKBP10), участвующих в дифференцировке остеобластов (WNT1, CREB3L1, SP7 и MBTPS2) и минерализации костной ткани (IFITM5), также приводят к НО различной степени тяжести [3]. Наиболее распространенными клиническими проявлениями заболевания, помимо хрупкости костей, являются голубые склеры, несовершенный дентиногенез, нарушение слуха. Существует несколько подходов к классификации НО, наиболее часто используется модифицированная клиническая классификация Sillence (I-V типы НО) с дополнительной информацией о конкретных молекулярных дефектах и их способе наследования. НО I типа (легкий недеформирующий) является наиболее распространенным, с голубыми склерами и небольшим количеством переломов, преимущественно в детском возрасте. НО II типа описывают как тяжелый перинатально-летальный с грубыми деформациями. Для данного типа характерны переломы основания черепа, позвонков и длинных трубчатых костей, а также снижение жизненной емкости легких [4]. НО III типа (прогрессивно деформирующий) характеризуется большим количеством переломов, низким ростом и выраженными скелетными деформациями. НО IV типа имеет широкую клиническую вариабельность и умеренную степень деформации. Данные четыре типа заболевания являются основными и составляют до 95% всех типов НО [5]. V тип (среднетяжелый с оссификацией межкостной мембраны предплечья) впервые был описан в литературе в 2000 г., характеризуется формированием гиперпластической костной мозоли и кальцификацией мембраны костей предплечья. Согласно литературным данным, возникновение гипертрофической костной мозоли иногда является спонтанным явлением, не связанным с предшествующими операциями и переломами, а также встречается реже, чем оссификация межкостной мембраны и вывих головки лучевой кости [6]. Главной задачей медикаментозного лечения НО является увеличение МПК при помощи антирезорбтивной (бисфосфонаты, деносумаб), анаболической (терипаратид, абалопаратид, гормон роста) или комбинированной (ромосозумаб) терапии. В настоящее время азотсодержащие бисфосфонаты признаны золотым стандартом лечения несовершенного остеогенеза в детском возрасте, за счет чего существенно снижается число переломов, пациенты сохраняют мобильность, социальную адаптацию, достигают совершеннолетия [7][8]. При этом возникает закономерный вопрос о необходимости и показаниях к продолжению терапии во взрослом возрасте. Ряд публикаций описывают увеличение показателей МПК у взрослых пациентов на фоне продолжения лечения БФ, но до сих пор не ясно, оказывают ли данные препараты влияние на риск переломов и другие клинические и лабораторные параметры [9][10].
ЦЕЛЬ
Оценка эффективности терапии бисфосфонатами у взрослых пациентов с несовершенным остеогенезом.
МАТЕРИАЛЫ И МЕТОДЫ
Дизайн исследования
Продольное сравнительное исследование пациентов с диагнозом «несовершенный остеогенез».
Критерии соответствия
В исследование включались взрослые пациенты с диагнозом «несовершенный остеогенез». Диагноз был установлен на основании клинической картины и результатов молекулярно-генетической диагностики. Основными клиническими проявлениями были множественные переломы костей скелета при незначительной травме, деформации конечностей и грудной клетки, голубое окрашивание склер. Молекулярно-генетическая диагностика включала в себя секвенирование с применением таргетной NGS-панели «Заболевания соединительной ткани», содержащей 492 гена.
Условия проведения
Исследование было проведено на базе клиники Башкирского государственного медицинского университета.
Продолжительность исследования
Период включения пациентов в исследование: 11.2021–08.2023 гг. Всем пациентам проводилась оценка уровня хронического болевого синдрома в костях при помощи визуально-аналоговой шкалы (ВАШ); оценка дисплазии соединительной ткани по модифицированной таблице Т.И. Кадуриной [11]. Диспластические изменения включали в себя гипермобильность суставов, кифосколиотическую деформацию позвоночника, деформацию грудной клетки, хруст в суставах, вальгусную установку стоп, пролапс митрального клапана и ряд висцеральных признаков, имеющие диагностическую ценность, выраженную в баллах. При сумме баллов от 9 до 14 ДСТ оценивалась как легкая, свыше 15 баллов — выраженная. Исследование МПК проводилось с применение рентгеновской абсорбциометрии (DXA) на аппарате Lunar prodigy advance (GE HealthCare, USA), с расчетом абсолютных значений и значений Z-критерия. Повторная оценка показателей уровня болевого синдрома и денситометрии осуществлялась через 12 месяцев.
Описание медицинского вмешательства
Пациенты с уровнем z-критерия менее -2,0, а также умеренным постоянным болевым синдромом более 5 баллов по ВАШ получили однократное введение золедроновой кислоты 5 мг на 100 мл физиологического раствора внутривенно капельно (длительность инфузии составляла не менее 15 минут).
Исходы исследования
Основной исход исследования: эффективность терапии БФ у взрослых пациентов с НО оценивалась по уменьшению уровня болевого синдрома в костях с умеренного постоянного до легкой боли, а также увеличению уровня показателей МПК и z-критерия по результатам рентгеновской денситометрии.
Дополнительные исходы исследования: корреляционная связь между степенью выраженности фенотипических признаков ДСТ и уровнем болевого синдрома в костях; отсутствие статистически значимых различий в уровне болевого синдрома у пациентов получавших и не получавших БФ ранее.
Анализ в подгруппах
Пациенты были исследованы в подгруппах, сформированных в зависимости от: типа НО (I, III, IV, V); наличия терапии БФ до 18 лет; наличия терапии золедроновой кислотой в рамках исследования.
Методы регистрации исходов
Для регистрации основных и дополнительных исходов исследования применялись: оценка уровня хронического болевого синдрома в костях при помощи визуально-аналоговой шкалы; оценка дисплазии соединительной ткани по модифицированной таблице Т.И. Кадуриной; исследование МПК с применение рентгеновской абсорбциометрии (DXA) на аппарате Lunar prodigy advance (GE HealthCare, USA) с расчетом абсолютных значений и значений Z-критерия; статистический анализ данных с использованием программного обеспечения Ms.Excel 2021 и GraphPad Prism 8.
Этическая экспертиза
Все этапы исследования были подробно и доступно изложены всем участникам, получено добровольное информированное согласие. Данное исследование осуществлено в полном соответствии с Хельсинкской декларацией (1964) и одобрено локальным этическим комитетом Башкирского государственного медицинского университета (протокол №8 от 23.10.2021).
Статистический анализ
Принципы расчета размера выборки: размер выборки предварительно не рассчитывался.
Методы статистического анализа данных: статистический анализ данных был выполнен с использованием программного обеспечения Ms.Excel 2021 и GraphPad Prism 8. Нормальность распределения оценивалось при помощи критерия Колмогорова-Смирнова. Для сравнения показателей между группами применялись: t-критерий Стьюдента, U-критерий Манна-Уитни, Критерий Краскела-Уоллиса, критерий Уилкоксона (с уровнем статистической значимости при p≤0,05). Анализ взаимосвязи между переменными проводился с расчетом коэффициентов корреляции Пирсона и Спирмена. Интерпретация силы корреляционной зависимости осуществлялась в соответствии со шкалой Чеддока.
РЕЗУЛЬТАТЫ
Объекты (участники) исследования
В исследование были включены 45 пациентов с несовершенным остеогенезом, среди которых 20 (44,4%) были мужчинами и 25 (55,6%) — женщины. Медиана возраста участников составила 32 года [ 23; 40,5]. По результатам молекулярно-генетического исследования у 36 (80%) пациентов были идентифицированы мутации причинных генов НО. Выявленные мутации, а также типы НО представлены в таблице 1. У 29 (64%) больных были обнаружены мутации в генах COL1A1 и COL1A2, ассоциированные с I, III и IV типами заболевания. II тип заболевания (перинатально-летальный) является одной из наиболее тяжелых форм НО, приводящей к смерти после рождения, поэтому не был представлен в когорте взрослых пациентов. У 3 пациентов выявлена мутация гена IFITM5, характерная для НО V типа [12]. Один пациент имел мутацию PLOD2 (синдром Брука). Также в когорте пациентов была обнаружена редкая мутация гена P3H1. У одного из пациентов выявлены мутации генов TGFB1 и SGMS2, характерные для кольцевого поражения свода черепа с хрупкостью костей [13][14]. Пациенты с данными мутациями в неколлагеновых генах имели I и IV типы заболевания. Клинические характеристики пациентов представлены в таблице 2.
Таблица 1. Выявленные мутации в генах, ассоциированных с несовершенным остеогенезом
|
Тип НО |
Название типа |
Количество пациентов |
Гены |
|
I |
Легкий недеформирующий |
21 |
COL1A1, COL1A2, P3H1, LRP5, PLOD2, TGFB1, SGMS2 |
|
III |
Умеренно тяжелый прогрессивно деформирующий |
6 |
COL1A1 |
|
IV |
Среднетяжелый вариабельный |
5 |
COL1A1, COL1A2, CRTAP |
|
V |
Среднетяжелый с оссификацией межкостной мембраны предплечья |
4 |
IFITM5, LAMB3 |
Таблица 2. Характеристики исследуемых пациентов с разными типами несовершенного остеогенеза
|
Все |
I тип НО |
III тип НО |
IV тип НО |
V тип НО |
|
|
Общее количество, n |
45 |
29 |
8 |
5 |
3 |
|
Мужчины, n (%) |
20 (44,4%) |
14 (48,3%) |
3 (37,5%) |
2 (40%) |
1 (33,3%) |
|
Женщины, n (%) |
25 (55,6%) |
15 (51,7%) |
5 (62,5%) |
3 (60%) |
2 (66,7%) |
|
Возраст, лет |
32 [ 23; 40,5] |
32 [ 21; 38] |
27,5 [ 23,5; 38,5] |
41 [ 33; 42] |
30 [ 28; 47] |
|
Рост, см |
155 [ 138;168,5] |
164 [ 151; 170] |
108,5 [ 100; 127,5] |
140 [ 139; 152] |
136 [ 100; 140] |
|
Вес, кг |
55,5±16,65 |
62±14,3 |
36,9±10,9 |
52,8±16,8 |
47±11,5 |
|
ИМТ, кг/м² |
25,27±5,45 |
23,6±4,6 |
28,5±5,9 |
26,3±4,5 |
30,8±8,2 |
|
Количество переломов |
15 [ 10; 32] |
11 [ 10; 20] |
45 [ 30; 60] |
20 [ 20; 40] |
30 [ 15; 50] |
|
ДСТ, баллы |
11 [ 9; 15] |
12 [ 9,5; 14,5] |
12,5 [ 8,5; 16,5] |
12 [ 11; 14,5] |
10 [ 5; 21] |
|
Голубые склеры, n (%) |
41 (91,1%) |
27 (93%) |
8 (100%) |
4 (80%) |
2 (66,7%) |
|
Нарушение слуха, n (%) |
14 (31,1%) |
11 (37,9%) |
1 (37,5%) |
2 (40%) |
0 |
|
Гипермобильность суставов, n (%) |
26 (57,8%) |
21 (72,4%) |
2 (25%) |
2 (40%) |
1 (33,3%) |
|
Патология зубной эмали, n (%) |
32 (71,1%) |
17 (58,6%) |
8 (100%) |
4 (80%) |
3 (100%) |
|
ВАШ, баллы |
5 [ 3; 6] |
4 [ 3; 6] |
5,5 [ 4; 6] |
5 [ 4,5; 5,5] |
6 [ 2; 6] |
|
МПК, г/см² |
0,996±0,16 |
1,048±0,12 |
0,828±0,1 |
1,01±0,27 |
0,917±0,12 |
|
z-критерий |
-0,8±1,33 |
-0,67±1,04 |
-1,8±1,56 |
-0,14±2,15 |
-1,1±0,62 |
Основные результаты исследования
Статистически значимые различия наблюдались при сравнении ИМТ у пациентов с I и III (23,6±4,6; 28,5±5,9; p=0,0183), I и V (23,6±4,6; 30,8±8,2; p=0,014) типами НО. Наименьшее количество переломов встречалось при I типе (11 [ 10; 20]; p=0,002), различия с остальными типами НО также достигли уровня статистической значимости (p<0,05 для каждой пары сравнения). Статистически значимых различий уровней балльно-количественной оценки ДСТ, болевого синдрома по ВАШ и z-критерия между разными типами заболевания не наблюдалось. Наиболее выраженная боль в костях была при V типе и составляла 6 баллов по ВАШ [ 2; 8]. Болевой синдром костной локализации у пациентов с НО характеризуется хроническим течением и отсутствием прямой связи с предыдущими переломами. Клинические наблюдения указывают на персистирующий характер болевых ощущений в состоянии покоя с тенденцией к интенсификации после физической нагрузки. Прием нестероидных противовоспалительных препаратов (НПВП) приводит к уменьшению боли, однако анальгетический эффект носит краткосрочный характер, а длительная терапия препаратами данной группы сопряжена с риском развития осложнений. Несмотря на отсутствие значимых различий в уровнях z-критерия, у пациентов с легким недеформирующим I типом были выявлены наиболее высокие показатели МПК, достигшие уровня статистической значимости в сравнении с III типом (1,048±0,12; 0,828±0,1; p=1*10⁻⁴) и V типом заболевания (1,048±0,12; 0,917±0,12; p=1*10⁻⁴). Из 45 исследуемых 22 пациента (49%) ранее получали терапию БФ, а 23 пациента (51%) никогда не получали препараты данной группы (табл. 3).
Таблица 3. Анализ показателей денситометрии и болевого синдрома в группах, получавших и не получавших бисфосфонаты ранее
|
Параметр |
Лечение до 18 лет |
Общее |
I тип НО |
III тип НО |
IV тип НО |
V тип НО |
|
ВАШ, баллы |
БФ+ |
5 [ 4; 6] |
5 [ 3; 6] |
6 [ 4,5; 6] |
5 [ 4 ;6] |
- |
|
БФ- |
4 [ 3; 6] |
3,5 [ 3; 5,3] |
4,5 [ 2,5; 5,8] |
5 [ 5; 5] |
6 [ 2; 6] |
|
|
МПК, г/см² |
БФ+ |
1,003±0,14 |
1,018±0,09 |
0,826±0,09 |
1,167±0,2 |
- |
|
БФ- |
0,988±0,18 |
1,079±0,14 |
0,831±0,13 |
0,774±0,17 |
0,917±0,12 |
|
|
Z-критерий |
БФ+ |
-0,89±1,57 |
-0,86±1,06 |
-2,46±1,57 |
1,1±1,81 |
- |
|
БФ- |
-0,8±1,08 |
-0,47±1,01 |
-1,13±1,42 |
-2±0,71 |
-1,1±0,62 |
Среди пациентов, получивших БФ ранее, наиболее высокие уровни МПК наблюдались при I и IV типах НО. В другой группе наиболее высокие уровни МПК были выявлены только при I типе. Статистически значимых различий между показателями в исследуемых группах выявлено не было.
Следующим этапом исследования была проведена оценка уровня болевого синдрома и результатов денситометрии в динамике у взрослых пациентов с НО, независимо от лечения БФ ранее (табл. 4). Из 45 исследуемых всего 24 пациента получили однократную внутривенную инфузию золедроновой кислоты 5 мг в КБГМУ. Показаниями для введения БФ являлись: наличие переломов в течение года (бедренная кость, надколенник, кости голени, пальцы рук и ног, локтевая и лучевая кости), низкие показатели МПК по данным денситометрии (z-критерий<-2,0), наличие умеренного постоянного болевого синдрома в костях (ВАШ>5 баллов). 7 пациентов имели переломы в течение года, показатели болевого синдрома составили менее 5 баллов по ВАШ (легкая или умеренная непостоянная боль), а значение z-критерия было в пределах остеопении. У 17 пациентов наблюдался умеренный постоянный болевой синдром в костях (5 и более баллов по ВАШ). У 8 пациентов с НО по результатам денситометрии уровни z-критерия были менее -2,0. У 8 пациентов наблюдалось сочетание умеренного постоянного болевого синдрома в костях и низкие показатели z-критерия. 9 пациентов из 24 ранее не получали терапию БФ. При всех типах НО было выявлено увеличение показателей МПК и z-критерия на фоне лечения БФ. Улучшение результатов денситометрии также не зависело от лечения бисфосфонатами ранее. У пациентов, не получивших БФ, не наблюдалось статистически значимых различий уровня болевого синдрома и МПК в динамике через 12 месяцев.
Таблица 4. Анализ показателей денситометрии и болевого синдрома в группе пациентов, получивших однократное введение золедроновой кислоты
|
Общее N=24 |
I тип НО N=14 |
III тип НО N=7 |
IV тип НО N=2 |
V тип НО N=1 |
|
|
ВАШ до лечения |
6 [ 4; 6] |
5,5 [ 4; 6] |
6 [ 4; 6] |
5,5 [ 5; 6] |
6 |
|
ВАШ после лечения |
3 [ 2; 4] |
3 [ 2; 4] |
2 [ 2; 4] |
3,5 [ 2; 5] |
4 |
|
p-value |
<0,0001* |
0,0005* |
0,0156* |
- |
- |
|
МПК до лечения |
0,948±0,16 |
1,009±0,07 |
0,806±0,09 |
1,022±0,52 |
0,926 |
|
МПК после лечения |
0,961±0,15 |
1,014±0,07 |
0,838±0,07 |
1,032±0,49 |
0,931 |
|
p-value |
0,1088 |
0,5200 |
0,2017 |
- |
- |
|
Z-кр. до лечения |
-1,2±1,47 |
-0,99±0,99 |
-2,14±1,32 |
0,25±3,9 |
-0,6 |
|
Z-кр. после лечения |
-0,9±1,19 |
-0,74±0,89 |
-1,63±1,16 |
-0,15±2,9 |
-0,5 |
|
p-value |
0,0450* |
0,0834 |
0,1103 |
- |
- |
* p<0.05
Дополнительные результаты исследования
При проведении корреляционного анализа у пациентов с НО была обнаружена умеренная обратная корреляционная связь между МПК и количеством переломов (r=-0,488, p=0,001), но не с z-критерием. Количество переломов также коррелировало с ИМТ (r=0,337, p=0,024). Уровень болевого синдрома имел прямую умеренную корреляционную связь со степенью выраженности фенотипических признаков дисплазии соединительной ткани (r=0,408, p=0,005). Результаты представлены на рисунке 1.
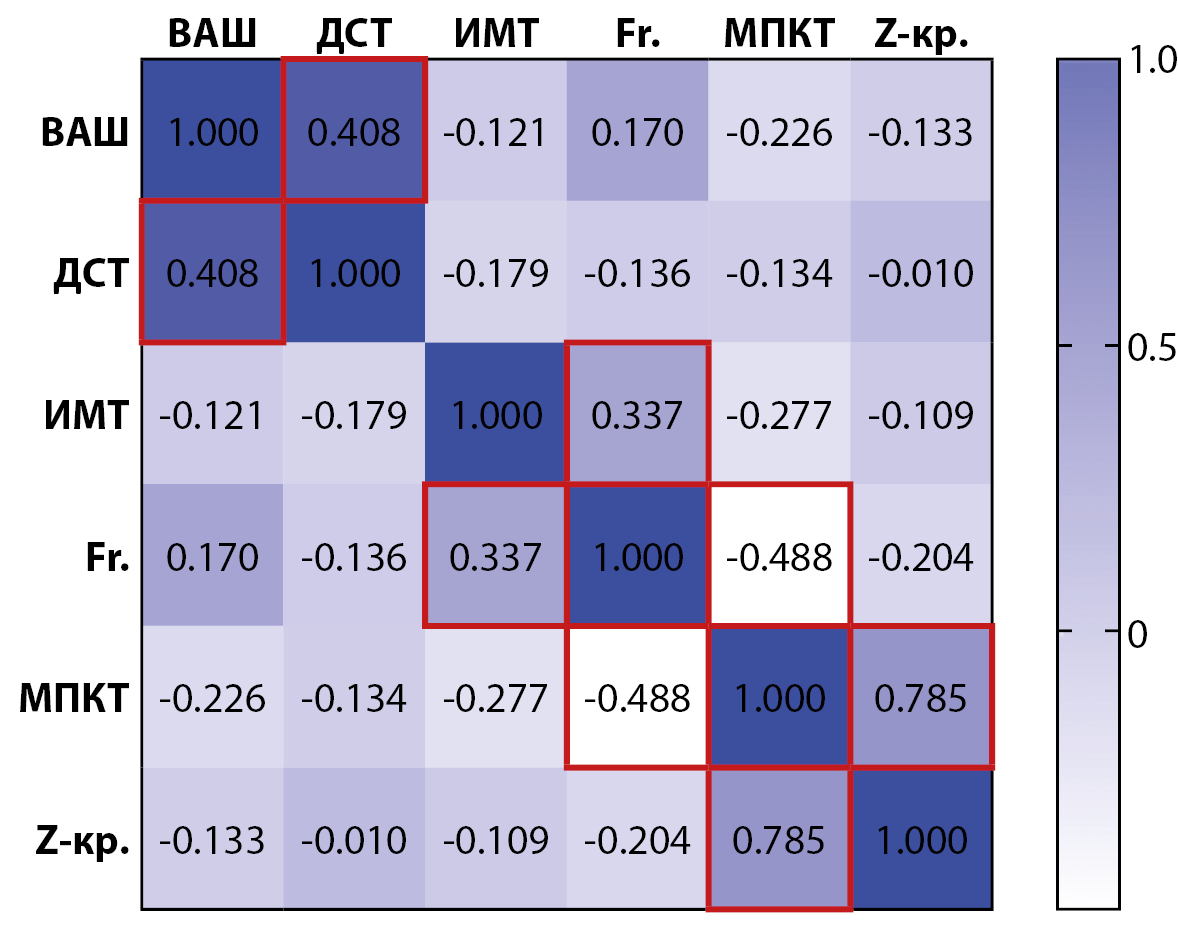
Рисунок 1. Результаты корреляционного анализа клинических параметров пациентов с НО.
Примечание: красным цветом выделены значимые корреляционные связи (р<0,05), ВАШ — уровень болевого синдрома по визуально-аналоговой шкале, ДСТ — количественная оценка дисплазии соединительной ткани по модифицированной таблице Т.И. Кадуриной, ИМТ — индекс массы тела, Fr. — количество переломов, МПК — минеральная плотность костной ткани, Z-кр. — z-критерий.
Нежелательные явления
В ходе проведения исследования медицинского вмешательства нежелательные явления отсутствовали.
ОБСУЖДЕНИЕ
Резюме основного результата исследования
У взрослых пациентов с НО сохраняются низкие уровни показателей МПК и z-критерия и присутствует болевой синдром в костях, не связанный с переломами. Интенсивность данных показателей не зависит от наличия предыдущей терапии бисфосфонатами. Лечение БФ является эффективным, так как наблюдалось статистически значимое увеличение МПК и z-критерия по результатам денситометрии, и статистически значимое уменьшение уровня болевого синдрома в костях.
Обсуждение основного результата исследования
В целом, полученные результаты согласуется с данными литературы. При исследовании 151 взрослого пациента с НО в Нидерландах, независимо от использования БФ, среднее МПК у пациентов с I типом составило — 1,77±1,08 г/см². Наибольшее количество переломов (в среднем, более 45) наблюдалось также при III типе [15]. По результатам другого исследования J.D. Hald наблюдалось сопоставимое среднее количество переломов у взрослых с I и IV типом НО, а также наибольшее количество переломов наблюдалось у взрослых с III типом НО. МПК была значительно ниже у пациентов с III типом, по сравнению с пациентами с IV типом заболевания (p<0,0001), однако существенных различий в МПК между пациентами с I и IV типами не наблюдалось [16].
Решения о применении БФ у пациентов в нашем исследовании зависели от наличия переломов в течение года, показателей денситометрии, а также от наличия умеренного постоянного болевого синдрома в костях (более 5 баллов по ВАШ), при отсутствии свежего перелома или другой травмы. Эффективность применения БФ с точки зрения снижения частоты переломов была продемонстрирована в нескольких исследованиях у пациентов детского возраста. Использование бисфосфонатов у взрослых с НО приводит к увеличению МПК, однако эффективность в снижении переломов остается неопределенной [17][18].
Болевой синдром в костях, не связанный с недавним переломом или другой травмой, в нашем исследовании наблюдался при всех типах НО и был наиболее выраженным у пациентов с V типом заболевания. Пациенты с этим типом никогда ранее не получали терапию данными препаратами. В литературе представлены результаты нескольких клинических исследований влияния БФ на болевой синдром у пациентов с НО. Снижение уровня боли и снижение частоты использования анальгетиков было отмечено только M.G. Seikaly в исследовании применения перорального алендроната у 17 детей с I, III и IV типами НО [19]. В 3-летнем рандомизированном двойном слепом плацебо-контролируемом исследовании G. Chevrel было выявлено увеличение болевого синдрома в группе, получающей алендронат, но не в группе плацебо [20]. В нескольких других исследованиях не было разницы в уровне боли и качестве жизни на фоне лечения БФ, но в данные исследования были включены пациенты только детского возраста. У 53 детей из Великобритании, получавших ризедронат в дозировке 0,2, 1 или 2 мг/кг в неделю, МПК поясничного отдела позвоночника значительно увеличилась только в группе, получавшей 2 мг/кг в неделю, а деформации длинных трубчатых костей уменьшились больше у детей, получавших 1 или 2 мг/кг в неделю, статистически значимых различий в уровнях болевого синдрома во всех группах не наблюдалось [21][22]. Таким образом, литературные данные о влиянии бисфосфонатов на уровень болевого синдрома в костной ткани и количество переломов носят противоречивый характер.
При проведении корреляционного анализа у пациентов с НО была выявлена умеренная обратная корреляционная связь между количеством переломов и уровнем МПК, но не с z-критерием. Это говорит о необходимости поиска новых подходов в интерпретации значений результатов денситометрии для данной когорты пациентов. Количество переломов и ИМТ пациентов также имели прямую умеренную корреляционную связь. Это может быть связано преимущественно с низким ростом пациентов с НО, который может быть обусловлен кифосколиотической деформацией позвоночника, компрессионными переломами позвоночника или рецидивирующими переломами длинных трубчатых костей. Выраженные деформации скелета приводят к снижению физической активности данных пациентов, что в свою очередь оказывает влияние на формирование избыточной массы тела. Согласно литературным данным, также предполагается, что избыточная передача сигналов трансформирующего фактора роста бета 1 может нарушать процессы пролиферации хондроцитов и тормозить их терминальную дифференцировку [23].
Уровень болевого синдрома в костях по ВАШ имел прямую умеренную корреляцию со степенью выраженности фенотипических признаков дисплазии у пациентов с НО. Боль в костях, вызванная травмой или переломом, по крайней мере изначально вызвана механическим искажением механочувствительных сенсорных нервных волокон в кости. С точки зрения механизма возникновения боли в костях без предшествующей травмы в литературе описано влияние чрезмерной активности остеокластов при резорбции кости, которая создает низкий уровень pH, стимулирующий кислоточувствительные ионные каналы, экспрессируемые сенсорными нервными волокнами, иннервирующими кость [24][25]. Вторым механизмом, который играет важную роль в усилении как острой, так и хронической боли в костях, является сенсибилизация костных ноцицепторов, активируемая брадикинином, эндотелином, эпидермальным фактором роста, нейротрофическим фактором, полученным из глиальных клеток, гистамином, фактором роста нервов, простагландинами, фактором некроза опухоли и фактором роста эндотелия сосудов. При данной сенсибилизации наблюдается усиленная реакция ноцицепторов даже на небольшие количества кислоты, выделяемой остеокластами, а также на простагландины и брадикинин, выделяемые поврежденными тканями, что в свою очередь приводит к увеличению передачи болевых сигналов в спинной и головной мозг [26, 27]. Также в литературе описано влияние эктопического прорастания нервов при переломах костей, даже при условии нормального заживления. По мере того, как сломанная кость обычно заживает и мозоль рассасывается, эти вновь выросшие нервные волокна обрезаются, так что после полного заживления кости ее иннервация возвращается к нормальному состоянию. Однако в случаях травмированной или больной кости, когда нормальное или быстрое заживление кости не происходит, это эктопическое разрастание нерва не отсекается, и травмированные или больные части кости остаются гипериннервируемыми. Данный механизм может влиять на переход от острой к хронической боли в костях у пациентов со скелетными дисплазиями [28][29].
Ограничения исследования
Небольшой объем выборки пациентов, короткий срок наблюдения, нерандомизированное назначение лечения.
ЗАКЛЮЧЕНИЕ
Таким образом, у взрослых пациентов с НО сохраняются сохраняются сниженные показатели МПК показателей МПК и z-критерия, а также присутствует умеренный постоянный болевой синдром в костях, не связанный с переломами. При этом не выявлено значимых различий в уровнях МПК и болевого синдрома в зависимости от наличия лечения БФ в анамнезе. Основными показаниями для продолжения терапии БФ являются наличие переломов в течение года, уровни z-критерия -2,0 и менее, наличие умеренного постоянного болевого синдрома в костях (ВАШ более 5 баллов). У пациентов с НО была выявлена умеренная обратная корреляционная связь между количеством переломов и ИМТ, количеством переломов и МПК, но не с z-критерием. Это говорит о необходимости поиска новых подходов в интерпретации значений результатов денситометрии для пациентов с НО.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источник финансирования. Рукопись подготовлена на личные средства авторского коллектива.
Участие авторов. Валеева Д.И. — сбор и обработка материалов, анализ полученных данных, написание текста; Тюрин А.В. — концепция и дизайн исследования, анализ полученных данных; Хусаинова Р.И. — концепция и дизайн исследования.
Конфликт интересов. Авторы данной статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
Список литературы
1. Marom R, Rabenhorst BM, Morello R. Osteogenesis imperfecta: an update on clinical features and therapies. Eur J Endocrinol. 2020;183(4):R95-R106. https://doi.org/10.1530/EJE-20-0299
2. Forlino A, Marini JC. Osteogenesis imperfecta. Lancet. 2016;387(10028):1657-71. https://doi.org/10.1016/S0140-6736(15)00728-X
3. Aksornthong S, Patel P, Komarova SV. Osteoclast indices in osteogenesis imperfecta: systematic review and meta-analysis. JBMR Plus. 2024;8(11):ziae112. https://doi.org/10.1093/jbmrpl/ziae112
4. Малыгина А.А., Гребенникова Т.А., Тюльпаков А.Н., Белая Ж.Е. Несовершенный остеогенез как причина летального исхода. Остеопороз и остеопатии. 2018;21(1):23-27. https://doi.org/10.14341/osteo9733
5. Westerheim I, Cormier-Daire V, Gilbert S, O’Malley S, Keen R. Osteogenesis Imperfecta: A study of the patient journey in 13 European countries. Orphanet J Rare Dis. 2024;19(1):331. https://doi.org/10.1186/s13023-024-03345-0
6. Гребенникова Т.А., Гаврилова А.О., Тюльпаков А.Н., Тарбаева Н.В., Белая Ж.Е., Мельниченко Г.А. Первое в России описание клинического случая несовершенного остеогенеза v типа с тяжелыми деформациями скелета, обусловленного мутацией с.119С>T в гене IFITM5. Остеопороз и остеопатии. 2019;22(2):32-3. https://doi.org/10.14341/osteo12103
7. Vuorimies I, Toiviainen-Salo S, Hero M, Mäkitie O. Zoledronic acid treatment in children with osteogenesis imperfecta. Horm Res Paediatr. 2011;75(5):346-53. https://doi.org/10.1159/000323368
8. Kumar C, Panigrahi I, Somasekhara Aradhya A, Meena BL, Khandelwal N. Zoledronate for Osteogenesis imperfecta: evaluation of safety profile in children. J Pediatr Endocrinol Metab. 2016;29(8):947-52. https://doi.org/10.1515/jpem-2015-0351
9. Scheres LJJ, van Dijk FS, Harsevoort AJ, van Dijk ATH, Dommisse AM, Janus GJM, et al. Adults with osteogenesis imperfecta: Clinical characteristics of 151 patients with a focus on bisphosphonate use and bone density measurements. Bone Rep. 2018;8:168-172. https://doi.org/10.1016/j.bonr.2018.04.009
10. Liu W, Lee B, Nagamani SCS, Nicol L, Rauch F, Rush ET, et al. Approach to the Patient: Pharmacological Therapies for Fracture Risk Reduction in Adults With Osteogenesis Imperfecta. J Clin Endocrinol Metab. 2023;108(7):1787-1796. https://doi.org/10.1210/clinem/dgad035
11. Тюрин А.В., Давлетшин Р.А., Муратова Р.М. Роль фенотипов дисплазии соединительной ткани в оценке риска развития соматической патологии. Казанский медицинский журнал. 2014; 95(4):501-505. https://doi.org/10.17816/KMJ1830
12. Tyurin A, Merkuryeva E, Zaripova A, Markova T, Nagornova T, Dantsev I, et al. Does the c.-14C>T Mutation in the IFITM5 Gene Provide Identical Phenotypes for Osteogenesis Imperfecta Type V? Data from Russia and a Literature Review. Biomedicines. 2022;10(10):2363. https://doi.org/10.3390/biomedicines10102363
13. Валеева ДИ, Хусаинова РИ, Хусаинова ЛН, Тюрин АВ. Наследственные заболевания человека со скелетной патологией – молекулярный патогенез и клиническая характеристика. Медицинский совет. 2024;18(5):202–213. https://doi.org/10.21518/ms2024-138
14. Merkuryeva Е, Мarkova T, Tyurin A, Valeeva D, Kenis V, Sumina M, et al. Clinical and Genetic Characteristics of Calvarial Doughnut Lesions with Bone Fragility in Three Families with a Reccurent SGMS2 Gene Variant. Int J Mol Sci. 2023;24(9):8021 https://doi.org/10.3390/ijms24098021
15. Zapata-Cornelio FY, Jin Z, Barton DC, Jones AC, Wilcox RK. A methodology for the generation and non-destructive characterisation of transverse fractures in long bones. Bone Rep. 2018;8:221-228. https://doi.org/10.1016/j.bonr.2018.04.007
16. Hald JD, Folkestad L, Harslf T, Lund AM, Duno M, Jensen JB, et al. Skeletal phenotypes in adult patients with osteogenesis imperfecta-correlations with COL1A1/COL1A2 genotype and collagen structure. Osteoporos Int. 2016;27(11):3331-3341. https://doi.org/10.1007/s00198-016-3653-0
17. Lindahl K, Åström E, Rubin CJ, Grigelioniene G, Malmgren B, Ljunggren Ö, et al. Genetic epidemiology, prevalence, and genotype-phenotype correlations in the Swedish population with osteogenesis imperfecta. Eur J Hum Genet. 2015;23(8):1112. https://doi.org/10.1038/ejhg.2015.129
18. Wekre LL, Eriksen EF, Falch JA. Bone mass, bone markers and prevalence of fractures in adults with osteogenesis imperfecta. Arch Osteoporos. 2011;6(1):31-8. https://doi.org/10.1007/s11657-011-0054-z
19. Seikaly MG, Kopanati S, Salhab N, Waber P, Patterson D, Browne R, et al. Impact of alendronate on quality of life in children with osteogenesis imperfecta. J Pediatr Orthop. 2005;25(6):786-91. https://doi.org/10.1097/01.bpo.0000176162.78980.ed
20. Chevrel G, Schott AM, Fontanges E, Charrin JE, Lina-Granade G, Duboeuf F, et al. Effects of oral alendronate on BMD in adult patients with osteogenesis imperfecta: a 3-year randomized placebo-controlled trial. J Bone Miner Res. 2006;21(2):300-6. https://doi.org/10.1359/JBMR.051015
21. Bishop N, Harrison R, Ahmed F, Shaw N, Eastell R, Campbell M, et al. A randomized, controlled dose-ranging study of risedronate in children with moderate and severe osteogenesis imperfecta. Journal of Bone and Mineral Research. 2010;25(1):32–40. https://doi.org/10.1359/jbmr.090712
22. Bishop N, Adami S, Ahmed SF, Antón J, Arundel P, Burren CP, et al. Risedronate in children with osteogenesis imperfecta: a randomised, double-blind, placebo-controlled trial. The Lancet. 2013;382(9902):1424–1432 https://doi.org/10.1016/S0140-6736(13)61091-0
23. Yang T, Grafe I, Bae Y, Chen S, Chen Y, Bertin TK, et al. E-selectin ligand 1 regulates bone remodeling by limiting bioactive TGF-β in the bone microenvironment. Proc Natl Acad Sci U S A. 2013;110(18):7336-41. https://doi.org/10.1073/pnas.1219748110
24. Nencini S, Ringuet M, Kim DH, Chen YJ, Greenhill C, Ivanusic JJ. Mechanisms of nerve growth factor signaling in bone nociceptors and in an animal model of inflammatory bone pain. Mol Pain. 2017;13:1744806917697011. https://doi.org/10.1177/1744806917697011
25. Ghilardi JR, Röhrich H, Lindsay TH, Sevcik MA, Schwei MJ, Kubota K, et al. Selective Blockade of the Capsaicin Receptor TRPV1 Attenuates Bone Cancer Pain. The Journal of Neuroscience. 2005;25(12):3126–3131. https://doi.org/10.1523/JNEUROSCI.3815-04.2005
26. Denk F, Bennett DL, McMahon SB. Nerve Growth Factor and Pain Mechanisms. Annu Rev Neurosci. 2017;40(1):307–325. https://doi.org/10.1146/annurev-neuro-072116-031121
27. Koewler NJ, Freeman KT, Buus RJ, Herrera MB, Jimenez-Andrade JM, Ghilardi JR, et al. Effects of a Monoclonal Antibody Raised Against Nerve Growth Factor on Skeletal Pain and Bone Healing After Fracture of the C57BL/6J Mouse Femur. Journal of Bone and Mineral Research. 2007;22(11):1732–1742. https://doi.org/10.1359/jbmr.070711
28. Mantyh PW. Mechanisms that drive bone pain across the lifespan. Br J Clin Pharmacol. 2019;85(6):1103–1113. https://doi.org/10.1111/bcp.13801
29. Chapurlat RD, Gensburger D, Jimenez-Andrade JM, Ghilardi JR, Kelly M, Mantyh P. Pathophysiology and medical treatment of pain in fibrous dysplasia of bone. Orphanet J Rare Dis. 2012;7(Suppl 1):S3 https://doi.org/10.1186/1750-1172-7-S1-S3
Об авторах
Д. И. ВалееваРоссия
Валеева Диана Ильдаровна, ассистент кафедры внутренних болезней и клинической психологии
ул. Ленина, 3, Уфа, Респ. Башкортостан, 450008
Р. И. Хусаинова
Россия
Хусаинова Рита Игоревна, д.б.н., профессор
Уфа
A. B. Тюрин
Тюрин Антон Викторович, д.м.н., доцент
Уфа
Дополнительные файлы
|
|
1. Рисунок 1. Результаты корреляционного анализа клинических параметров пациентов с НО. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(318KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Валеева Д.И., Хусаинова Р.И., Тюрин A.B. Оценка эффективности терапии бисфосфонатами взрослых пациентов с несовершенным остеогенезом. Остеопороз и остеопатии. 2025;28(3):4-11. https://doi.org/10.14341/osteo13210
For citation:
Valeeva D.I., Khusainova R.I., Tiurin A.V. Evaluation of the efficacy of bisphosphonate therapy in adult patients with osteogenesis imperfecta. Osteoporosis and Bone Diseases. 2025;28(3):4-11. (In Russ.) https://doi.org/10.14341/osteo13210
JATS XML

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).





































