Перейти к:
Применение бисфосфонатов для профилактики остеопоротических переломов у женщин с остеопенией в постменопаузе: систематический обзор и метаанализ
https://doi.org/10.14341/osteo13150
Аннотация
ОБОСНОВАНИЕ. Отсутствие достаточной систематизации данных по применению бисфосфонатов для первичной профилактики остеопоротических переломов (ОП) у женщин в постменопаузе с остеопенией побудило нас провести систематический обзор с метаанализом публикаций, посвященных данной проблеме.
ЦЕЛЬ. Изучить влияние бисфосфонатов на минеральную плотность кости (МПК) и переломы у женщин в постменопаузе с остеопенией.
МАТЕРИАЛЫ И МЕТОДЫ. При первичном отборе было найдено 1140 потенциально подходящих статей. Из первоначально идентифицированных результатов был проведен метаанализ 13 исследований. Дизайн отобранных для метаанализа исследований соответствовал рандомизированным контролируемым исследованиям (РКИ).
РЕЗУЛЬТАТЫ. В среднем исследуемые препараты бисфосфонатов по сравнению с плацебо увеличивали МПК поясничного отдела позвоночника на 5,54 % (95 % ДИ 4,44–6,63, I2=93,65 %), общую МПК бедра на 4,53 % (95 % ДИ 3,2–5,86, I2=96,32 %), МПК шейки бедра на 3,63 % (95 % ДИ 1,5–5,75, I2 = 95,9 %), МПК всего тела на 3,25 % (95 % ДИ 2,28–4,22, I2 = 87,87 %), МПК проксимального отдела бедра на 4,76 % (95 % ДИ 3,43–6,08, I2 = 88,64 %). Выявлено статистически значимое влияние бисфосфонатов на низкоэнергетические переломы (ОР 0,62; 95 % ДИ 0,49–0,77), клинические переломы позвонков (ОР 0,51; 95 % ДИ 0,38–0,69), а также рентгенологически подтверждённые переломы позвонков (ОР 0,63; 95 % ДИ 0,4–0,98).
ЗАКЛЮЧЕНИЕ. Полученные результаты позволяют заключить, что бисфосфонаты (алендронат, золедроновая кислота, ибандронат, резедронат) обладают положительным терапевтическим эффектом, и их назначение оправдано у женщин в постменопаузе с остеопенией для профилактики ОП и увеличения МПК.
Ключевые слова
Для цитирования:
Юренева С.В., Аверкова В.Г. Применение бисфосфонатов для профилактики остеопоротических переломов у женщин с остеопенией в постменопаузе: систематический обзор и метаанализ. Остеопороз и остеопатии. 2024;27(1):21-34. https://doi.org/10.14341/osteo13150
For citation:
Yureneva S.V., Averkova V.G. Bisphosphonates for the prevention of osteoporotic fractures in postmenopausal women with osteopenia: a systematic review and meta-analysis. Osteoporosis and Bone Diseases. 2024;27(1):21-34. (In Russ.) https://doi.org/10.14341/osteo13150
ОБОСНОВАНИЕ
Остеопороз является серьезной медико-социальной проблемой из-за его последствий в виде патологических переломов, которые приводят к инвалидизации и смертности пожилого населения [1]. С учетом прогнозируемого увеличения продолжительности жизни во всем мире профилактику остеопоротических переломов (ОП) можно рассматривать как одну из приоритетных задач здравоохранения.
Известно, что большинство ОП случаются у людей, имеющих показатели минеральной плотности кости (МПК), соответствующие остеопении, а не остеопорозу, особенно в сочетании с другими факторами риска (такими как пожилой возраст или женский пол) [2].
Бисфосфонаты — препараты для лечения остеопороза, показавшие свою эффективность в отношении увеличения МПК и профилактики ОП [3–5]. Данные об эффективности применения бисфосфонатов при остеопении для первичной профилактики ОП не были достаточно систематизированы. Целью настоящего обзора было изучить влияние бисфосфонатов на МПК, маркеры метаболизма костной ткани и переломы у женщин в постменопаузе с остеопенией.
ЦЕЛЬ
Изучить влияние бисфосфонатов на минеральную плотности кости (МПК), маркеры метаболизма костной ткани и переломы у женщин в постменопаузе с остеопенией.
МАТЕРИАЛЫ И МЕТОДЫ
Поиск публикаций и отбор исследований
Систематический поиск исследований и соответствующих статей проводили в базах данных PubMed, EMBASE, Google Scholar и Кокрановская библиотека (Cochrane Library) в соответствии с требованиями для систематических обзоров и метаанализов (PRISMA) [6]. Ключевые слова для поиска включали: (osteopenia), AND (low bone density), AND (fractures, bone), AND (bone markers), AND (alendronate, OR risedronic acid, OR zoledronic acid, OR clodronic acid, OR pamidronate, ibandronic acid, OR 6-amino-1-hydroxyhexane-1,1-diphosphonate). Последний поиск осуществлялся 25 сентября 2023 г.
Критерии включения/исключения
Критериями включения в метаанализ были:
- рандомизированное плацебо-контролируемое исследование эффективности бисфосфонатов в отношение МПК и профилактики переломов;
- участники — женщины в постменопаузе старше 45 лет с остеопенией (T-критерий от -1,0 до2,5 по данным двухэнергетической рентгеноденситометрии (DXA));
- нижний порог длительности наблюдения в исследованиях 12 месяцев.
Критериями невключения в метаанализ были:
- дубликаты статей;
- исследования на животных;
- невозможность получить доступ к полному тексту публикации по результатам исследования.
Извлечение, синтез данных исследований и оценка их качества
При первичном отборе исследований с помощью вышеуказанных баз данных и поисковых запросов было получено 1140 потенциально подходящих работ. После их проверки по критериям включения/невключения и удаления дубликатов для дальнейшего анализа были отобраны 844 публикации. При анализе заголовков и аннотаций статей поставленной в нашей работе цели соответствовали 24 публикации. 11 исследований были исключены из дальнейшего анализа по причине отсутствия доступа к полнотекстовым копиям статей по результатам исследования, а также из-за отсутствия заданных данных. Таким образом, в метаанализ вошли 13 исследований (рис. 1).

Рисунок 1. Алгоритм отбора публикаций для метаанализа.
Статистический анализ
Метаанализ проводили с использованием среды для статистических вычислений R 4.3.1 (R Foundation for Statistical Computing, Vienna, Austria) и пакета metafor 4.2-0. Для получения метааналитических оценок использовали модели со случайными эффектами (mixed-effects models). Оценка статистической гетерогенности была выполнена с использованием критерия χ² Пирсона и индекса гетерогенности I2. Метаанализ различий средних значений показателей в исследуемой и контрольной (плацебо) группах был выполнен по данным о средних значениях со стандартными отклонениями.
РЕЗУЛЬТАТЫ
1. Характеристика исследований, включенных в метаанализ
Синопсис исследований [7–19], включенных в метаанализ, представлен в таблице 1. Это были рандомизированные контролируемые исследования (РКИ), результаты которых были опубликованы с 1995 по 2023 гг. В исследованиях были оценены эффекты бисфосфонатов (алендронат, золедроновая кислота, ибандронат, ризедронат) на МПК, ОП, маркеры метаболизма костной ткани; в некоторых исследованиях были представлены данные по нежелательным явлениям (НЯ) на фоне терапии бисфосфонатами и данные о приверженности к лечению.
Таблица 1. Синопсис исследований, включенных в метаанализ
|
Авторы, год публикации |
Дизайн |
Количество участников (исследуемые/контроль) |
Средний возраст участников (исследуемые/контроль |
Терапия |
Длительность наблюдения |
Конечные точки |
|
SR Cummings, (1998) |
РКИ |
2214/2218 |
67,6 (6,2)/67,6 (6,1) |
алендронат 5 мг/сут в течение двух лет, алендронат 10 мг/сут в последующие 2 года в сравнении с плацебо |
48 мес |
ОП, МПК, рост, НЯ |
|
HA Pols (1999) |
РКИ |
950/958 |
63,0 (39–84)/63,0 (40–82) |
алендронат 10 мг/сут в сравнении с плацебо |
12 мес |
ОП, МПК, маркеры метаболизма костной ткани, НЯ |
|
Yen et al. (2000) |
РКИ |
24/22 |
59±4,7/60,3±6,5 |
алендронат 10 мг/сут в сравнении с плацебо |
12 мес |
МПК, НЯ |
|
McClung et al. (2004) |
РКИ |
59/74 |
58,2±8,6/57,9±8,6 |
ибандроновая кислота 2,5 мг/сут по сравнению с плацебо |
24 мес |
МПК |
|
Quandt et al. (2005) |
РКИ |
1878/1859 |
67,6/67,8 |
алендронат 5 мг/сут в течение двух лет, алендронат 10 мг/сут в последующие 2,5 года в сравнении с плацебо |
54 мес |
ОП |
|
Valimaki et al. (2007) |
РКИ |
114/56 |
66,1 (6,8)/65,4 (6,8) |
Ризедронат 5 мг/сут в сравнении с плацебо |
26 мес |
МПК, НЯ |
|
McClung et al. (2009) -1 |
РКИ |
198/202 |
59,9±8,0/60,5±8,0 |
Золедроновая кислота 5 мг 2 раза/сут (10 мг) и золедроновая кислота 5 мг/сут в сравнении с плацебо |
24 мес |
МПК, маркеры метаболизма костной ткани, НЯ |
|
McClung et al. (2009) -2 |
РКИ |
77/83 |
53,7±3,6/53,4±3,8 |
ибадроновая кислота 150 мг/мес в сравнении с плацебо |
12 мес |
МПК, НЯ |
|
Grey et al. (2012) |
РКИ |
20/21 |
62 (8)/67 (8) |
золедроновая кислота 5 мг/сут в сравнении с плацебо |
60 мес |
МПК, маркеры метаболизма костной ткани, НЯ |
|
Grey et al. (2017) |
РКИ |
41/34 |
66±8/63±8 |
золедроновая кислота 5 мг/сут (в/в) в сравнении с плацебо |
60 мес |
МПК, маркеры метаболизма костной ткани |
|
Reid et al. (2018) |
РКИ |
1000/1000 |
71±5,0/71±5,1 |
золедроновая кислота 5 мг/сут (в/в) 18 мес в сравнении с плацебо |
72 мес |
ОП, МПК, маркеры метаболизмам костной ткани, НЯ |
|
Sestak et al. (2019) |
РКИ |
59/74 |
60,8 (7,67)/59,7 (12,5) |
ризедронат 35 мг/нед в сравнении с плацебо |
60 мес |
МПК, НЯ |
|
Zhou et al. (2020) |
РКИ |
62/61 |
83,16±3,09/83,92±2,85 |
алендронат 70 мг/нед в сравнении с плацебо |
18 мес |
ОП, МПК, маркеры метаболизмам костной ткани, НЯ |
Примечание: ОП — остеопоротические переломы;
МПК — минеральная плотность кости; НЯ — нежелательные явления.
1.1 Риск систематической ошибки
В нашем исследовании мы использовали следующую систему оценки риска: низкий риск, умеренный риск и высокий риск. Семь отобранных исследований имели низкий риск систематической ошибки [7][8][13][15–18], одно – высокий риск систематической ошибки [18]. Еще пяти исследованиям был присвоен неизвестный риск систематической ошибки, поскольку не было получено достаточно информации для его расчетов [9–12][14].
2. Процентное изменение МПК поясничного отдела позвоночника
Влияние бисфосфонатов (алендронат, золедроновая кислота, ибандронат, ризедронат) на МПК поясничного отдела позвоночника в сравнении с плацебо изучали в десяти РКИ (табл. 2, рис. 2). В среднем исследуемые препараты бисфосфонатов по сравнению с плацебо увеличивали МПК поясничного отдела позвоночника на 5,54% (95% ДИ 4,44–6,63, I2=93,65%).
Таблица 2. Результаты метаанализа влияния бисфосфонатов
на МПК поясничного отдела позвоночника
|
Исследование |
Бисфосфонаты |
Плацебо |
WMD |
95% CI |
Weight (%) |
||
|
n |
M (SD) |
n |
M (SD) |
||||
|
Zoledronate |
|||||||
|
McClung (2009) |
198 |
5,1 (3,827) |
202 |
-1,32 (3,809) |
6,42 |
5,67; 7,17 |
11 |
|
Grey (2012) |
20 |
5,42 (1,79) |
21 |
-0,86 (2,89) |
6,28 |
4,82; 7,74 |
9,6 |
|
Grey (2017) |
41 |
3,16 (5,8) |
34 |
-2 (5,36) |
5,16 |
2,63; 7,69 |
7,2 |
|
Reid (2018) |
755 |
7,42 (5,26) |
750 |
-1,03 (5,55) |
8,45 |
7,9; 9 |
11,3 |
|
Subtotal (p<0,001) |
6,83 |
5,47; 8,18 |
|||||
|
Q (3)=25,5, p<0,001 τ=1,21 I²=85,76% |
|||||||
|
Risedronate |
|||||||
|
Valimaki (2007) |
106 |
4,49 (3,91) |
53 |
-0,05 (3,93) |
4,54 |
3,25; 5,83 |
10 |
|
Sestak (2019) |
59 |
3,96 (6,52) |
74 |
-0,26 (5,05) |
4,22 |
2,2; 6,24 |
8,3 |
|
Subtotal (p<0,001) |
4,45 |
3,36; 5,54 |
|||||
|
Q (1)=0,068, p=0,794 τ=0 I²=0,00% |
|||||||
|
Alendronate |
|||||||
|
Pols (1999) |
877 |
5 (3,2) |
903 |
0,1 (3,4) |
4,9 |
4,59; 5,21 |
11,5 |
|
Yen (2000) |
24 |
7 (2,23) |
22 |
-0,59 (2) |
7,59 |
6,37; 8,81 |
10,2 |
|
Subtotal (p<0.001) |
6,18 |
3,54; 8,81 |
|||||
|
Q (1)=17,5, p<0,001 τ=1,85 I²=94,29% |
|||||||
|
Ibandronate |
|||||||
|
McClung (2004) |
106 |
1,88 (3,95) |
102 |
-1,37 (3,45) |
3,25 |
2,24; 4,26 |
10,6 |
|
McClung (2009) |
77 |
3,58 (3,72) |
83 |
-0,43 (3,8) |
4,01 |
2,84; 5,18 |
10,3 |
|
Subtotal (p<0,001) |
3,57 |
2,81; 4,34 |
|||||
|
Q (1)=0,935, p=0,334 τ=0 I²=0,00% |
|||||||
|
Overall (p<0,001) |
5,54 |
4,44; 6,63 |
|||||
|
Q(9)=172,6, p<0,001 τ=1,63 I²=93,65% |
|||||||

Рисунок 2. Результаты метаанализа влияния бисфосфонатов
на МПК поясничного отдела позвоночника.
Примечание: M (SD) — средняя арифметическая (стандартное отклонение);
WMD — средняя арифметическая взвешенная;
95% CI — 95% доверительный интервал (ДИ); Weight (%) — вес (%).
3. Процентное изменение общей МПК бедра
Влияние бисфосфонатов (алендронат, золедроновая кислота, ибандронат, ризедронат) на общую МПК бедра в сравнении с плацебо изучали в семи РКИ (табл. 3, рис. 3). В среднем исследуемые препараты бисфосфонатов по сравнению с плацебо увеличивали общую МПК бедра на 4,53% (95% ДИ 3,2–5,86, I2=96,32%).
Таблица 3. Результаты метаанализа влияния бисфосфонатов на общую МПК бедра
|
Исследование |
Бисфосфонаты |
Плацебо |
WMD |
95% CI |
Weight (%) |
||
|
n |
M (SD) |
n |
M (SD) |
||||
|
Zoledronate |
|||||||
|
McClung (2009) |
198 |
2,91 (2,913) |
202 |
-1,45 (2,871) |
4,36 |
3,79; 4,93 |
15,0 |
|
Grey (2012) |
20 |
0,88 (1,41) |
21 |
-4,44 (2,46) |
5,32 |
4,1; 6,54 |
13,6 |
|
Grey (2017) |
41 |
1,93 (3,77) |
34 |
-3,51 (2,54) |
5,44 |
4; 6,88 |
13,1 |
|
Reid (2018) |
755 |
3,54 (4,12) |
750 |
-3,97 (5,03) |
7,51 |
7,05; 7,97 |
15,1 |
|
Subtotal (p<0,001) |
5,69 |
4,27; 7,11 |
|||||
|
Q(3)=73,9, p<0,001 τ=1,359 I²=92,64% |
|||||||
|
Risedronate |
|||||||
|
Sestak (2019) |
59 |
0,99 (4,68) |
74 |
-2,71 (3,19) |
3,7 |
2,3; 5,1 |
13,2 |
|
Subtotal (p<0,001) |
3,7 |
2,3; 5,1 |
|||||
|
Alendronate |
|||||||
|
Pols (1999) |
527 |
3,1 (3,5) |
537 |
0,1 (3) |
3 |
2,61; 3,39 |
15,2 |
|
Subtotal (p<0.001) |
3 |
2,61; 3,39 |
|||||
|
Ibandronate |
|||||||
|
McClung (2009) |
77 |
1,49 (2,31) |
83 |
-0,93 (2,04) |
2,42 |
1,74; 3,1 |
14,8 |
|
Subtotal (p<0,001) |
2,42 |
1,74; 3,1 |
|||||
|
Overall (p<0,001) |
4,53 |
3,2; 5,86 |
|||||
|
Q (6)=258,5, p<0,001 τ=1,726 I²=96,32% |
|||||||

Рисунок 3. Результаты метаанализа влияния бисфосфонатов на общую МПК бедра.
Примечание: M (SD) — средняя арифметическая (стандартное отклонение);
WMD — средняя арифметическая взвешенная; 95%
CI — 95% доверительный интервал (ДИ); Weight (%) — вес (%).
4. Процентное изменение МПК шейки бедра
Влияние бисфосфонатов (алендронат, золедроновая кислота, ибандронат) на МПК шейки бедра в сравнении с плацебо изучали в четырех РКИ (табл. 4, рис. 4). В среднем исследуемые препараты бисфосфонатов по сравнению с плацебо увеличивали МПК шейки бедра на 3,63% (95% ДИ 1,5–5,75, I2=95,9%).
Таблица 4. Результаты метаанализа влияния бисфосфонатов на МПК шейки бедра
|
Исследование |
Бисфосфонаты |
Плацебо |
WMD |
95% CI |
Weight (%) |
||
|
n |
M (SD) |
n |
M (SD) |
||||
|
Zoledronate |
|||||||
|
McClung (2009) |
198 |
2,2 (4,137) |
202 |
-1,35 (4,093) |
3,55 |
2,74; 4,36 |
25,8 |
|
Subtotal (p<0,001) |
3,55 |
2,74; 4,36 |
|||||
|
Alendronate |
|||||||
|
Pols (1999) |
863 |
2,3 (4,5) |
884 |
-0,2 (4,5) |
2,5 |
2,08; 2,92 |
26,5 |
|
Yen (2000) |
24 |
6,83 (3,24) |
22 |
-0,19 (2,83) |
7,02 |
5,27; 8,77 |
22,7 |
|
Subtotal (p=0,038) |
4,68 |
0,25; 9,1 |
|||||
|
Q (1)=24,1, p<0,001 τ=3,129 I²=95,85% |
|||||||
|
Ibandronate |
|||||||
|
McClung (2009) |
77 |
1,09 (2,82) |
83 |
-0,75 (4,1) |
1,84 |
0,76; 2,92 |
25 |
|
Subtotal (p<0,001) |
1,84 |
0.76; 2,92 |
|||||
|
Overall (p<0,001) |
3,63 |
1,5; 5,75 |
|||||
|
Q (3)=30,5, p<0,001 τ=2,095 I²=95,9% |
|||||||

Рисунок 4. Результаты метаанализа влияния бисфосфонатов на МПК шейки бедра.
Примечание: M (SD) — средняя арифметическая (стандартное отклонение);
WMD — средняя арифметическая взвешенная;
95% CI — 95% доверительный интервал (ДИ); Weight (%) — вес (%).
5. Процентное изменение МПК всего тела (Total Body BMD)
Влияние бисфосфонатов (золедроновая кислота) на МПК всего тела в сравнении с плацебо изучали в трех РКИ (табл. 5, рис. 5). В среднем исследуемые препараты бисфосфонатов по сравнению с плацебо увеличивали МПК всего тела на 3,25% (95% ДИ 2,28–4,22, I2=87,87%).
Таблица 5. Результаты метаанализа влияния бисфосфонатов на МПК всего тела
|
Исследование |
Бисфосфонаты |
Плацебо |
WMD |
95% CI |
Weight (%) |
||
|
n |
M (SD) |
n |
M (SD) |
||||
|
Zoledronate |
|||||||
|
Grey (2012) |
20 |
0,48 (1,14) |
21 |
-2,14 (1) |
2,62 |
1,96; 3,28 |
33,1 |
|
Grey (2017) |
41 |
-0,12 (2,144) |
34 |
-2,97 (1,89) |
2,85 |
1,94; 3,76 |
29,0 |
|
Reid (2018) |
755 |
1,95 (2,58) |
750 |
-2,16 (2,58) |
4,11 |
3,85; 4,37 |
37,9 |
|
Overall (p<0,001) |
3,25 |
2,28; 4,22 |
|||||
|
Q (2)=21,85, p<0,001 τ=0,795 I²=87,87% |
|||||||
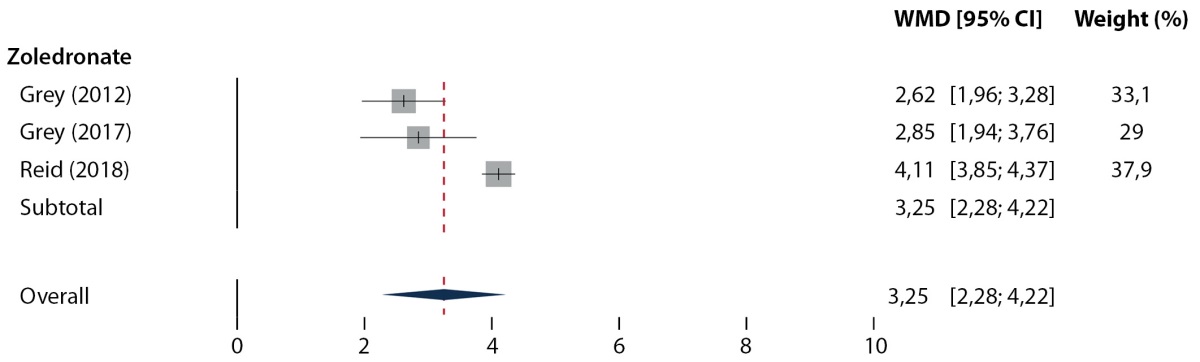
Рисунок 5. Результаты метаанализа влияния бисфосфонатов на МПК всего тела.
Примечание: M (SD) — средняя арифметическая (стандартное отклонение);
WMD — средняя арифметическая взвешенная;
95% CI — 95% доверительный интервал (ДИ); Weight (%) — вес (%).
6. Процентное изменение МПК проксимального отдела бедра
Влияние бисфосфонатов (алендронат, золедроновая кислота, ибандронат) на МПК проксимального отдела бедра в сравнении с плацебо изучали в четырех РКИ (табл. 6, рис. 6). В среднем исследуемые препараты бисфосфонатов по сравнению с плацебо увеличивали МПК проксимального отдела бедра на 4,76% (95% ДИ 3,43–6,08, I2=88,64%).
Таблица 6. Результаты метаанализа влияния бисфосфонатов
на МПК проксимального отдела бедра
|
Исследование |
Бисфосфонаты |
Плацебо |
WMD |
95% CI |
Weight (%) |
||
|
n |
M (SD) |
n |
M (SD) |
||||
|
Zoledronate |
|||||||
|
McClung (2009) |
198 |
4,83 (3,912) |
202 |
-1,15 (3,866) |
5,98 |
5,22; 6,74 |
28,2 |
|
Subtotal (p<0,001) |
5,98 |
5,22; 6,74 |
|||||
|
Alendronate |
|||||||
|
Pols (1999) |
863 |
4,1 (5,2) |
884 |
0,4 (4,6) |
3,7 |
3,24; 4,16 |
29,9 |
|
Yen (2000) |
24 |
0,54 (3,77) |
22 |
-5,69 (4,36) |
6,23 |
3,86; 8,6 |
15,6 |
|
Subtotal (p<0,001) |
4,69 |
2,27; 7,11 |
|||||
|
Q (1)=4,235, p=0,04 τ=1,564 I²=76,39% |
|||||||
|
Ibandronate |
|||||||
|
McClung (2009) |
77 |
2,87 (3,3) |
83 |
-0,91 (3,25) |
3,78 |
2,76; 4,8 |
26,3 |
|
Subtotal (p<0,001) |
3,78 |
2,76; 4,8 |
|||||
|
Overall (p<0,001) |
4,76 |
3,43; 6,08 |
|||||

Рисунок 6. Результаты метаанализа влияния бисфосфонатов
на МПК проксимального отдела бедра.
Примечание: M (SD) — средняя арифметическая (стандартное отклонение);
WMD — средняя арифметическая взвешенная;
95% CI — 95% доверительный интервал (ДИ); Weight (%) — вес (%).
7. Переломы
Влияние бисфосфонатов (алендронат, золендроновая кислота) на риск ОП изучалось в трех РКИ. Выявлено статистически значимое влияние бисфосфонатов на низкоэнергетические переломы (ОР 0,62; 95% ДИ 0,49–0,77) (переломы позвонков, переломы бедра, запястья и других частей скелета, за исключением переломов плюсневых костей и пальцев, переломов костей черепа, костей лицевого черепа и нижней челюсти), клинические переломы позвонков ((ОР 0,51; 95% ДИ 0,38–0,69)), а также рентгенологически подтвержденные переломы позвонков (ОР 0,63; 95% ДИ 0,4–0,98) (табл. 7–9, рис. 7–9).
Таблица 7. Результаты метаанализа эффективности бисфосфонатов
в отношении профилактики клинических переломов позвонков
|
Исследование |
HR/RR |
95% CI |
Weight (%) |
|
Zoledronate |
|||
|
Reid (2018) |
0,41 |
0,22; 0,75 |
23,3 |
|
Subtotal (p=0,004) |
0,41 |
0,22; 0,75 |
|
|
Alendronate |
|||
|
Cummings (1998) |
0,56 |
0,39; 0,8 |
67,9 |
|
Quandt (2005) |
0,46 |
0,16; 1,17 |
8,8 |
|
Subtotal (p<0,001) |
0,55 |
0,39; 0,77 |
|
|
Q (1)=0,133, p=0,716 τ=0 I²=0,00% |
|||
|
Overall (p<0,001) |
0,51 |
0,38; 0,69 |
|
|
Q (2)=0,788, p=0,674 τ=0 I²=0,00% |
|||

Рисунок 7. Результаты метаанализа эффективности бисфосфонатов
в отношении профилактики клинических переломов позвонков.
Примечание: HR/RR — отношение рисков (ОР*)/относительный риск (ОР);
95% CI — 95% доверительный интервал (ДИ); Weight (%) — вес (%).
Таблица 8. Результаты метаанализа эффективности бисфосфонатов
в отношении профилактики рентгенологически подтвержденных переломов позвонков
|
Исследование |
HR/RR |
95% CI |
Weight (%) |
|
Zoledronate |
|||
|
Reid (2018) |
0,6 |
0,27; 1,37 |
30 |
|
Subtotal (p=0,218) |
0,6 |
0,27; 1,35 |
|
|
Alendronate |
|||
|
Quandt (2005) |
0,64 |
0,38; 1,1 |
70 |
|
Subtotal (p=0,1) |
0,64 |
0,38; 1,09 |
|
|
Overall (p=0,04) |
0,63 |
0,4; 0,98 |
|
|
Q (1)=0,017, p=0,896 τ=0 I²=0,00% |
|||

Рисунок 8. Результаты метаанализа эффективности бисфосфонатов
в отношении профилактики рентгенологически подтвержденных переломов позвонков.
Сокращения: HR/RR — отношение рисков (ОР*)/относительный риск (ОР);
95% CI — 95% доверительный интервал (ДИ); Weight (%) — вес (%).
Таблица 9. Результаты метаанализа эффективности бисфосфонатов
в отношении профилактики низкоэнергетических переломов
(переломы позвонков, переломы бедра, запястья и других частей скелета,
за исключением переломов плюсневых костей и пальцев,
переломов костей черепа, костей лицевого черепа и нижней челюсти)
|
Исследование |
HR/RR |
95% CI |
Weight (%) |
|
Zoledronate |
|||
|
Reid (2018) |
0,63 |
0,5; 0,79 |
94,9 |
|
Subtotal (p<0,001) |
0,63 |
0,5; 0,79 |
|
|
Alendronate |
|||
|
Quandt (2005) |
0,4 |
0,15; 1,08 |
5,1 |
|
Subtotal (p=0,069) |
0,4 |
0,15; 1,07 |
|
|
Overall (p=0,379) |
0,62 |
0,49; 0,77 |
|
|
Q (1)=0,772, p=0,896 τ=0 I²=0,00% |
|||

Рисунок 9. Результаты метаанализа эффективности бисфосфонатов
в отношении профилактики низкоэнергетических переломов
(переломы позвонков, переломы бедра, запястья и других частей скелета,
за исключением переломов плюсневых костей и пальцев,
переломов костей черепа, костей лицевого черепа и нижней челюсти).
Примечание: HR/RR — отношение рисков (ОР*)/относительный риск (ОР);
95% CI — 95% доверительный интервал (ДИ); Weight (%) — вес (%).
ОБСУЖДЕНИЕ
Бисфосфонаты широко используются как в нашей стране, так и во всем мире для лечения остеопороза. Снижение костного ремоделирования и частоты его активации является основой фармакологического действия данных препаратов на костную ткань [20]. Алендронат (первый зарегистрированный в РФ бисфосфонат для лечения остеопороза), золедроновая кислота (бисфосфонат III поколения, обладающий наибольшим сродством к гидроксиапатиту кости), а также ибандронат и ризедронат применяются и для лечения другой патологии костной ткани (в том числе при метастазах в костную ткань при онкологических заболеваниях). В последние годы возрос интерес к вопросу применения бисфосфонатов для первичной и вторичной профилактики ОП.
Мы провели систематический обзор и метаанализ изучения эффективности указанных бисфосфонатов в отношении увеличения МПК и профилактики ОП у женщин в постменопаузе с остеопенией. Полученные нами данные согласуются с результатами метаанализа 2022 г. [21], в котором были продемонстрированы статистически значимые эффекты лечения данной группы препаратов (а именно, алендроната, золедроната, ибандроната и резедроната) на увеличение МПК позвоночника, бедра и общей МПК всего тела.
В нашей работе были дополнены данные по влиянию двух бисфосфонатов (алендронат и золедроновая кислота) на профилактику ОП у женщин с остеопенией в постменопаузе. Нами было показано, что алендронат и золедроновая кислота существенно снижают риски клинических переломов позвонков, а также в целом снижают риски низкоэнергетических переломов и рентгенологически подтвержденных переломов позвонков по сравнению с плацебо.
Сильными сторонами нашего исследования является качественный отбор публикаций для метаанализа только высокой степени доказательности (плацебо-контролируемые РКИ, часть с двойным ослеплением). Ограничениями для нашего исследования стали: невозможность провести метаанализ влияния бисфосфонатов на маркеры метаболизма костной ткани, а также метаанализ нежелательных явлений на фоне терапии, поскольку во включенных исследованиях не было достаточно заданных данных.
ЗАКЛЮЧЕНИЕ
Основываясь на данных нашего исследования, можно заключить, что бисфосфонаты (алендронат, золедроновая кислота, ибандронат, резедронат) обладают положительным терапевтическим эффектом, и их назначение оправдано у женщин в постменопаузе с остеопенией для профилактики ОП и увеличения МПК.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источники финансирования. Работа выполнена по инициативе авторов без привлечения финансирования.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов.
Юренева С.В. — разработка концепции и дизайна исследования, редактирование и одобрение финальной версии рукописи; Аверкова В.Г. — получение, анализ данных и их интерпретация, написание текста статьи.
Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. Sànchez-Riera L, Wilson N. Fragility Fractures & Their Impact on Older People. Best Pract Res Clin Rheumatol. 2017;31(2):169-191. doi: 10.1016/j.berh.2017.10.001
2. Lindsay R, Silverman SL, Cooper C, et al. Risk of new vertebral fracture in the year following a fracture. JAMA. 2001;285(3):320-3. doi: 10.1001/jama.285.3.320
3. Sanderson J, Martyn-St James M, Stevens J, et al. Clinical effectiveness of bisphosphonates for the prevention of fragility fractures : A systematic review and network meta-analysis. Bone. 2016;89:52-58. doi: 10.1016/j.bone.2016.05.013
4. Deardorff WJ, Cenzer I, Nguyen B, Lee SJ. Time to Benefit of Bisphosphonate Therapy for the Prevention of Fractures Among Postmenopausal Women With Osteoporosis: A Meta-analysis of Randomized Clinical Trials. JAMA Intern Med. 2022;182(1):33-41. doi: 10.1001/jamainternmed.2021.6745
5. Кузнецова Л.В., Зазерская И.Е., Айламазян Э.К., Потин В.В. Сопоставление эффективности эстроген-гестагенных препаратов и алендроната в терапии остеопении у женщин постменопаузального возраста // Остеопороз и остеопатии. — 2007. — № 2. doi: 10.14341/osteo200727-12
6. Moher D, Liberati A, Tetzlaff J, et al. Preferred Reporting Items for Systematic Reviews and Meta-Analyses: the PRISMA statement. PLoS Med. 2009;6(7):e1000097. doi: 10.1371/journal.pmed.1000097
7. Cummings SR, Black DM, Thompson DE, et al. Effect of alendronate on risk of fracture in women with low bone density but without vertebral fractures: results from the Fracture Intervention Trial. JAMA. 1998;280(24):2077-82. doi: 10.1001/jama.280.24.2077
8. Pols HA, Felsenberg D, Hanley DA, Stepán J, et al. Multinational, placebo-controlled, randomized trial of the effects of alendronate on bone density and fracture risk in postmenopausal women with low bone mass: results of the FOSIT study. Fosamax International Trial Study Group. Osteoporos Int. 1999;9(5):461-8. doi: 10.1007/pl00004171
9. Yen ML, Yen BL, Jang MH, Hsu SH, et al. Effects of alendronate on osteopenic postmenopausal Chinese women. Bone. 2000;27(5):681-5. doi: 10.1016/s8756-3282(00)00384-7
10. McClung MR, Wasnich RD, Recker R, et al. Oral Ibandronate Study Group. Oral daily ibandronate prevents bone loss in early postmenopausal women without osteoporosis. J Bone Miner Res. 2004;19(1):11-8. doi: https://doi.org/10.1359/JBMR.0301202
11. Quandt SA, Thompson DE, Schneider DL, et al. Fracture Intervention Trial Research Group. Effect of alendronate on vertebral fracture risk in women with bone mineral density T scores of-1.6 to -2.5 at the femoral neck: the Fracture Intervention Trial. Mayo Clin Proc. 2005;80(3):343-9. doi: 10.4065/80.3.343
12. Välimäki MJ, Farrerons-Minguella J, Halse J, et al. Effects of risedronate 5 mg/d on bone mineral density and bone turnover markers in late-postmenopausal women with osteopenia: a multinational, 24-month, randomized, double-blind, placebo-controlled, parallel-group, phase III trial. Clin Ther. 2007;29(9):1937-49. doi: 10.1016/j.clinthera.2007.09.017
13. McClung M, Miller P, Recknor C, et al. Zoledronic acid for the prevention of bone loss in postmenopausal women with low bone mass: a randomized controlled trial. Obstet Gynecol. 2009;114(5):999-1007. doi: 10.1097/AOG.0b013e3181bdce0a
14. McClung MR, Bolognese MA, Sedarati F, et al. Efficacy and safety of monthly oral ibandronate in the prevention of postmenopausal bone loss. Bone. 2009;44(3):418-22. doi: 10.1016/j.bone.2008.09.011
15. Grey A, Bolland MJ, Horne A, Wattie D, et al. Five years of anti-resorptive activity after a single dose of zoledronate--results from a randomized double-blind placebo-controlled trial. Bone. 2012;50(6):1389-93. doi: 10.1016/j.bone.2012.03.016
16. Grey A, Bolland MJ, Horne A, et al. Duration of antiresorptive activity of zoledronate in postmenopausal women with osteopenia: a randomized, controlled multidose trial. CMAJ. 2017;189(36):E1130-E1136. doi: 10.1503/cmaj.161207
17. Reid IR, Horne AM, Mihov B, Stewart A, et al. Fracture Prevention with Zoledronate in Older Women with Osteopenia. N Engl J Med. 2018;379(25):2407-2416. doi: 10.1056/NEJMoa1808082
18. Sestak I, Blake GM, Patel R, Coleman RE, et al. Comparison of risedronate versus placebo in preventing anastrozole-induced bone loss in women at high risk of developing breast cancer with osteopenia. Bone. 2019;124:83-88. doi: 10.1016/j.bone.2019.04.016
19. Zhou J, Liu B, Qin MZ, Liu JP. Fall Prevention and Anti-Osteoporosis in Osteopenia Patients of 80 Years of Age and Older: A Randomized Controlled Study. Orthop Surg. 2020;12(3):890-899. doi: 10.1111/os.12701
20. Burr DB, Diab T, Koivunemi A, et al. Effects of 1 to 3 years’ treatment with alendronate on mechanical properties of the femoral shaft in a canine model: implications for subtrochanteric femoral fracture risk. J Orthop Res. 2009;27(10):1288-92. doi: 10.1002/jor.20895
21. Li J, Sun Y, Chen Z, Xie X, Gu F, Bi S, Yu T. Effects of Bisphosphonates Treatments in Osteopenic Older Women : A Systematic Review and Meta-Analysis. Front Pharmacol. 2022;13:892091. doi: 10.3389/fphar.2022.892091
Об авторах
С. В. ЮреневаРоссия
Светлана Владимировна Юренева, д. м. н., профессор
117997; ул. Академика Опарина, д. 4; Москва
Scopus Author ID: 56299444500
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
В. Г. Аверкова
Россия
Виктория Геннадьевна Аверкова, аспирант
Москва
Scopus Author ID: 57213597365
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Дополнительные файлы
|
|
1. Рисунок 1. Алгоритм отбора публикаций для метаанализа. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(317KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 2. Результаты метаанализа влияния бисфосфонатов на МПК поясничного отдела позвоночника. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(277KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 3. Результаты метаанализа влияния бисфосфонатов на общую МПК бедра. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(234KB)
|
Метаданные ▾ | |
|
|
4. Рисунок 4. Результаты метаанализа влияния бисфосфонатов на МПК шейки бедра. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(167KB)
|
Метаданные ▾ | |
|
|
5. Рисунок 5. Результаты метаанализа влияния бисфосфонатов на МПК всего тела. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(105KB)
|
Метаданные ▾ | |
|
|
6. Рисунок 6. Результаты метаанализа влияния бисфосфонатов на МПК проксимального отдела бедра. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(164KB)
|
Метаданные ▾ | |
|
|
7. Рисунок 7. Результаты метаанализа эффективности бисфосфонатов в отношении профилактики клинических переломов позвонков. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(136KB)
|
Метаданные ▾ | |
|
|
8. Рисунок 8. Результаты метаанализа эффективности бисфосфонатов в отношении профилактики рентгенологически подтвержденных переломов позвонков. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(127KB)
|
Метаданные ▾ | |
|
|
9. Рисунок 9. Результаты метаанализа эффективности бисфосфонатов в отношении профилактики низкоэнергетических переломов (переломы позвонков, переломы бедра, запястья и других частей скелета, за исключением переломов плюсневых костей и пальцев, переломов костей черепа, костей лицевого черепа и нижней челюсти). | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(123KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Юренева С.В., Аверкова В.Г. Применение бисфосфонатов для профилактики остеопоротических переломов у женщин с остеопенией в постменопаузе: систематический обзор и метаанализ. Остеопороз и остеопатии. 2024;27(1):21-34. https://doi.org/10.14341/osteo13150
For citation:
Yureneva S.V., Averkova V.G. Bisphosphonates for the prevention of osteoporotic fractures in postmenopausal women with osteopenia: a systematic review and meta-analysis. Osteoporosis and Bone Diseases. 2024;27(1):21-34. (In Russ.) https://doi.org/10.14341/osteo13150

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).






































